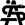Fachbeitrag 05/2024 - Kasabach-Merritt-Syndrom
- Titel Fachbeitrag: Laparoskopische Cholezystektomie für symptomatische Cholezystolithiasis (CCL) bei „Kasabach-Merritt-Syndrom“ (KMS)
- Ärzteblatt Ausgabe: ÄB 2024/05
- Autor: Dr. Stephan Arndt
Kaposi-Tumor-ähnliches Hämangioendotheliom –
fallspezifisches perioperatives Management
Foto: Adobe Stock | #399729635
S. Arndt1, C. Wex2, I. Häusler-Pliske2, D. Jechorek3, H. Krause4, Z. Halloul1, F. Meyer2
Sekundäreinreichung nach Erstveröffentlichung im Open Access Modus unter der Creative Commons Lizenz BY 4.0 beim „de-Gruyter-Verlag“
1 Arbeitsbereich Gefäßchirurgie; Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie
2 Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie
3 Institut für Pathologie
4 Abteilung Kinderchirurgie, Kindertraumatologie und Kinderurologie; Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie Universitätsklinikum Magdeburg Ä. ö. R.
S. Arndt1, C. Wex2, I. Häusler-Pliske2, D. Jechorek3, H. Krause4, Z. Halloul1, F. Meyer2
Sekundäreinreichung nach Erstveröffentlichung im Open Access Modus unter der Creative Commons Lizenz BY 4.0 beim „de-Gruyter-Verlag“
1 Arbeitsbereich Gefäßchirurgie; Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie
2 Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie
3 Institut für Pathologie
4 Abteilung Kinderchirurgie, Kindertraumatologie und Kinderurologie; Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie Universitätsklinikum Magdeburg Ä. ö. R.

Dr. med. Stephan Arndt (Foto: privat)

Das Kasabach-Merritt-Syndrom (KMS, ICD 10 D18.0, D69.5) beschreibt das Auftreten von Hämangioendotheliomen (Riesenhämangiome) mit darin ablaufender Thrombosierung, was über den Verbrauch von Gerinnungsfaktoren und Thrombozyten mit einer disseminierten intravasalen Gerinnung (Verbrauchskoagulopathie) einhergeht (1).
In diesem Fallbericht soll, basierend auf
i) selektiv eruierten Referenzen der aktuellen themenbezogenen medizinisch-wissenschaftlichen
Literatur und ihren Empfehlungen sowie
ii) eigenen klinischen Managementerfahrungen aus dem abdominal-chirurgischen Alltag,
die häufige elektive Cholezystektomie (CCE) bei einer symptomatischen Cholezystolithiasis unter der Koinzidenz des seltenen Krankheitsbildes eines KMS wissenschaftlich beispielhaft umrissen werden.
Eine 72-jährige Patientin stellte sich nach auswärtig vor 3 Monaten konservativ behandelter akuter Cholezystitis bei Cholezystolithiasis unter dem Wunsch einer elektiven Cholezystektomie in der hiesigen Einrichtung vor. Bekannt ist ein KMS des linken Arms, der linken oberen Thoraxapertur mit rezidivierenden Thrombophlebitiden des linken Armes und der Thoraxvenen. Anamnestisch besteht ein Zustand nach zahlreichen Blutungskomplikationen nach
- Zahnextraktionen,
- einer offen-chirurgischen Appendektomie 1962 (und)
- einer Sectio caesarea im Jahr 1968, bei welcher 60 Erythrozytenkonzentrate transfundiert werden mussten.
Ferner bestehen
- ein Zustand nach gastrointestinaler Blutung bei Mallory-Weiss-Syndrom 2006,
- eine chronische Anämie bei Vitamin-B12-Mangel,
- eine Typ-A-Gastritis,
- eine Hypothyreose,
- eine arterielle Hypertonie,
- eine beginnende Leberzirrhose,
- eine chronische Niereninsuffizienz – Stadium II (sowie)
- eine Makrolid- und Penicillinallergie.
An Hausmedikamenten wird L-Thyroxin, ein ACE-Hemmer, Hydrochlorothiazid und zur Vermeidung einer überschießenden Thrombozytenaggregation Plavix eingenommen. Die Patientin trug einen linksseitigen Armkompressionsstrumpf.
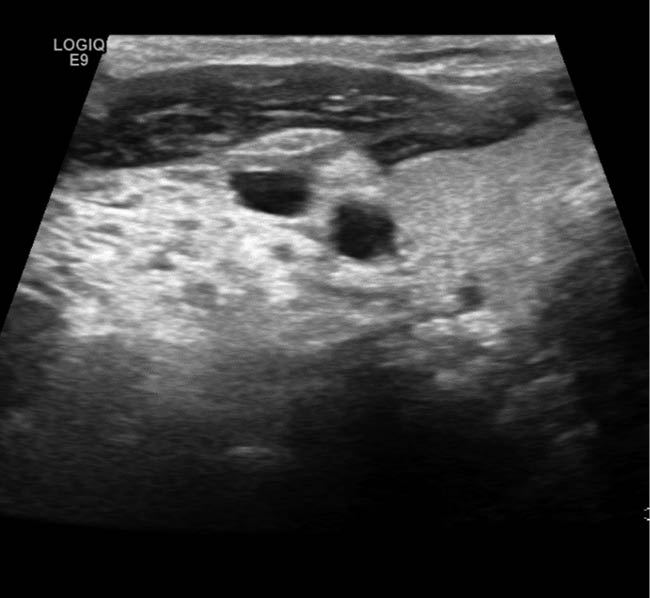
Aufgrund der symptomatischen Cholezystolithiasis nach stattgehabter akuter Cholezystitis wurde die Indikation zur elektiven laparoskopischen Cholezystektomie gestellt. An diagnostischen Verfahren wurden auswärts ein Angio-MRT (Abb. 1 – 4) des Oberbauches und eine Magnetresonanz-Cholangiopankreatikographie (MRCP) durchgeführt, welche eine Cholezystitis bei Cholezystolithiasis und eine beginnende Leberzirrhose nachweisen konnten. Im Rahmen der präoperativen Vorbereitung wurde eine Echokardiographie durchgeführt, in welchem eine Herzinsuffizienz infolge der Volumenbelastung durch die AV-Shunts i.R. des KMS und eine „Cirrhose cardiaque“ ausgeschlossen werden konnten. Als Marker einer intravasalen Gerinnungsaktivierung wurden erhöhte Prothrombinfragmente, D-Dimere und eine erniedrigte Antiplasmin-Konzentration sowie eine gesteigerte Fibrinolysekapazität detektiert. Eine sekundäre Thrombozytopenie oder eine Fibrinogen- und Faktor-XIII-Verminderung konnten ebenso wie das Vorliegen eines erworbenen von-Willebrand-Syndroms ausgeschlossen werden.
In einer hämostaseologischen Vorstellung wurde die Pausierung der Thrombozytenaggregationshemmung über 7 d unter „Bridging“ mittels niedermolekularem Heparin und eine medikamentöse Hemmung der Hyperfibrinolyse durch Tranexamsäure bis zum 3. postoperativen Tag bzw. in Abhängigkeit von Klinik und des hämostaseologischen perioperativen Monitorings empfohlen. Als perioperative Antibiotikaprophylaxe wurde Imipenem eingesetzt. Der Kameratrokar wurde entsprechend der aus dem Angio-MRT bekannten linksseitigen Ausprägung der Gefäßmalformationen (Abb. 1 – 4) in typischer Nabelposition platziert.
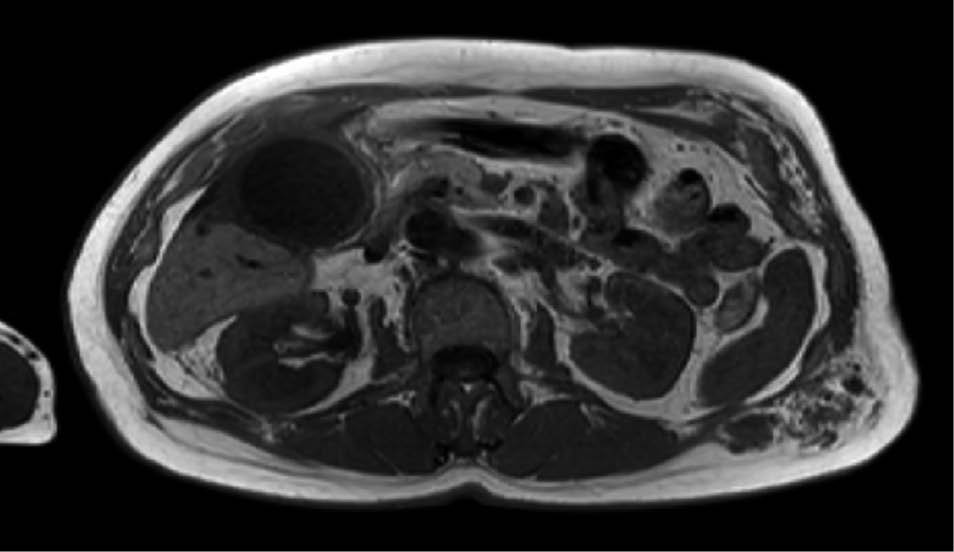
Abb. 1: Angio-MRT mit Transversalschnitt des oberen Abdomens auf Höhe der Gallenblase: Neben der hydroptisch geschwollenen und wandverdickten Gallenblase -> Hämangioendotheliom
im Bereich der ventralen und dorsalen linken Rumpfwand
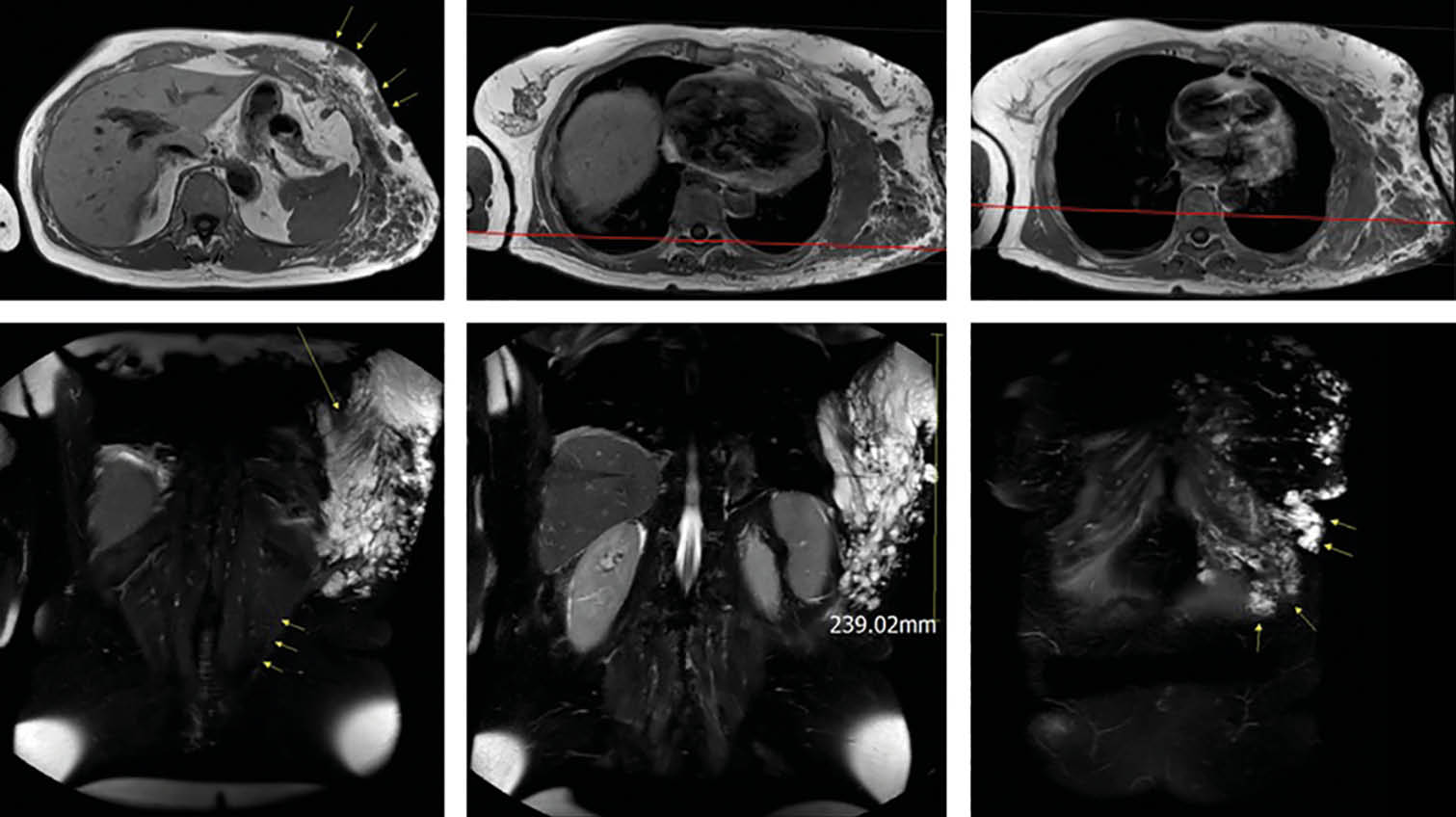
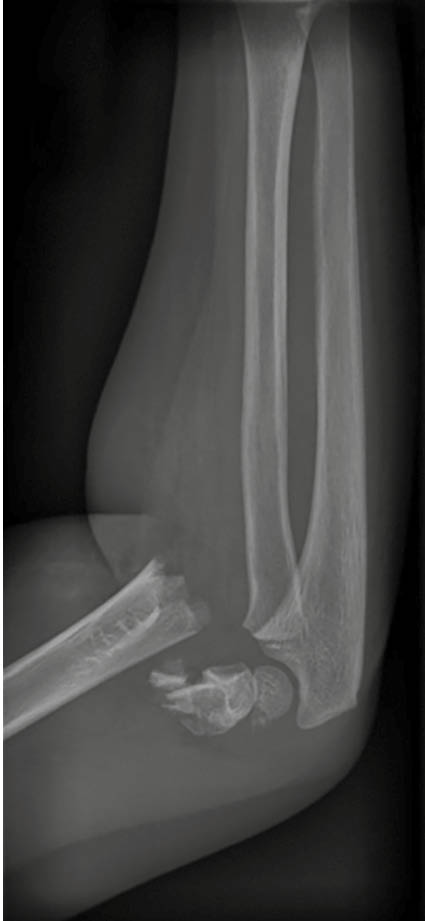
Abb. 2: MRT:
A) T1 axial kutan am Arcus
B) T1 axial – Befund am
M. latissimus dorsi
C) T1 axial – Hauptbefund an der hinteren Axillarlinie
D) T2 coronar – M.-latissimus-dorsi-Linie
E) T2 koronar – Hauptbefund an der hinteren Axillarlinie
F) T2 koronar – kutan am Arcus
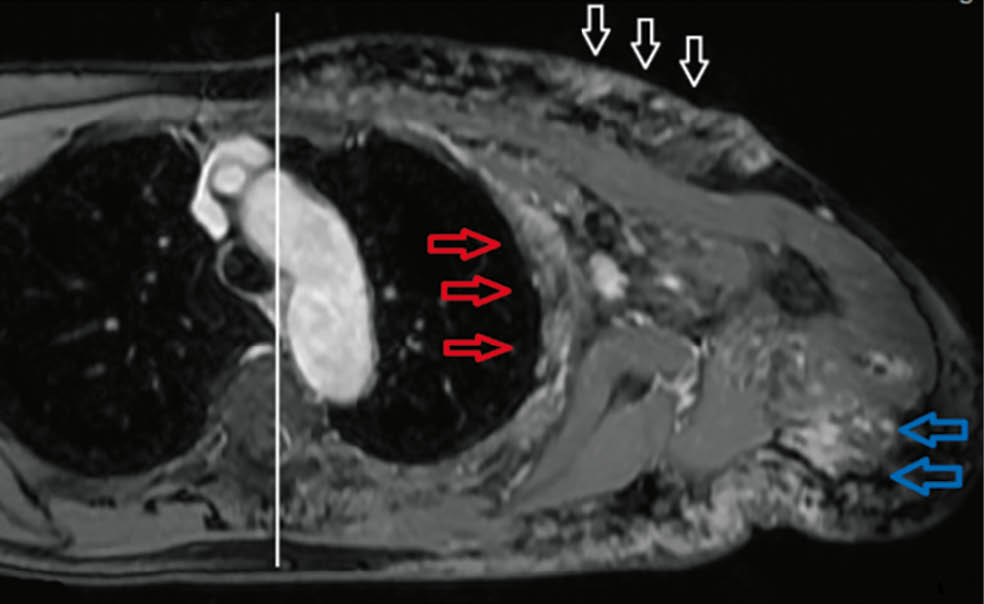
Abb. 3: KM-verstärkte fettunterdrückte axiale T1-Sequenz:
Tubulär-granuläre KM-anreichende Befunde mit Beteiligung der Interkostalmuskulatur (rote Pfeile), der Oberarmmuskulatur (blaue Pfeile) und der Kutis (weiße Pfeile). Auffällige Begrenzung der Malformation auf einen Quadranten des Körperstammes
(siehe weiße Mittellinie)
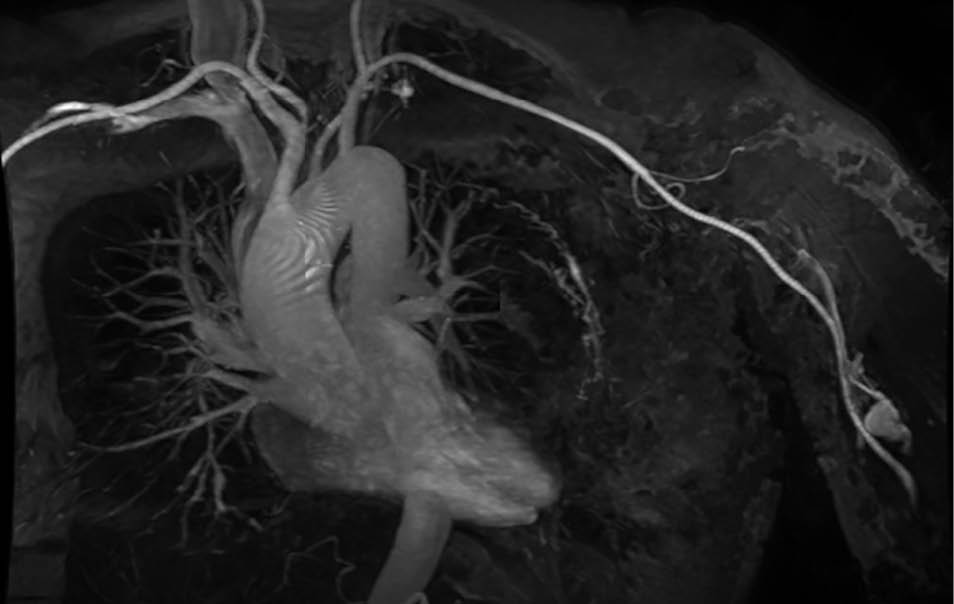
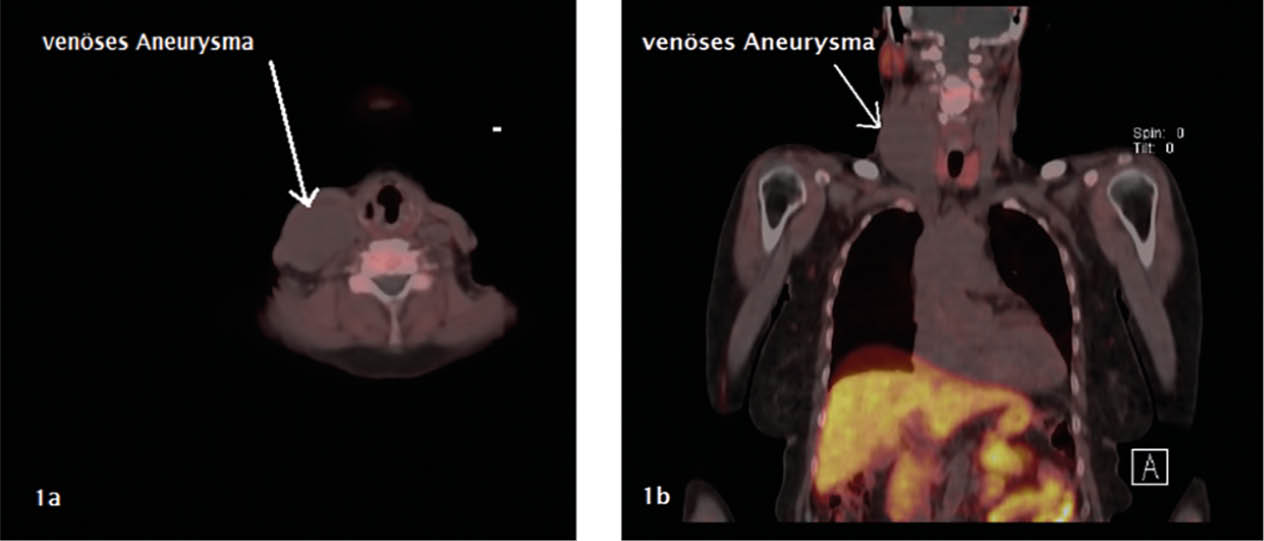
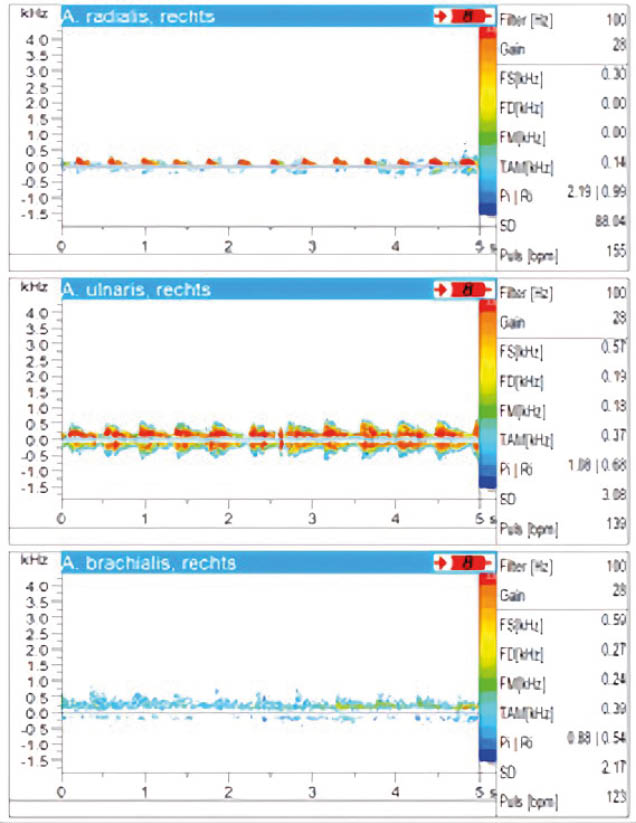
Abb. 4: MR-Angiografie
(koronare Projektion) – betonte Intercostalarterien
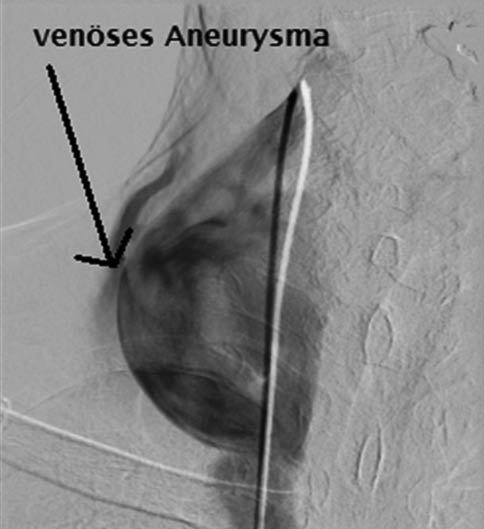
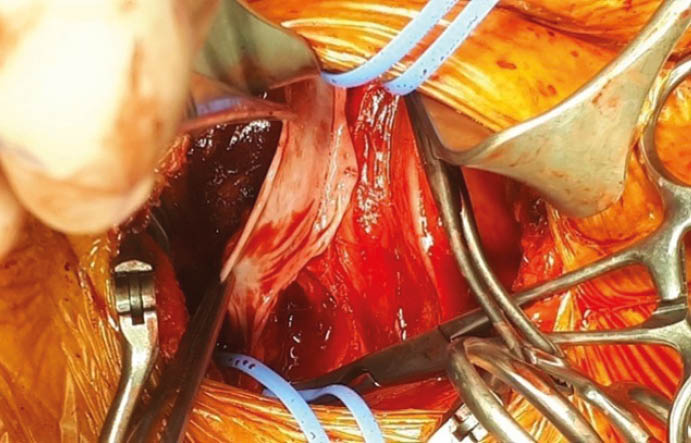
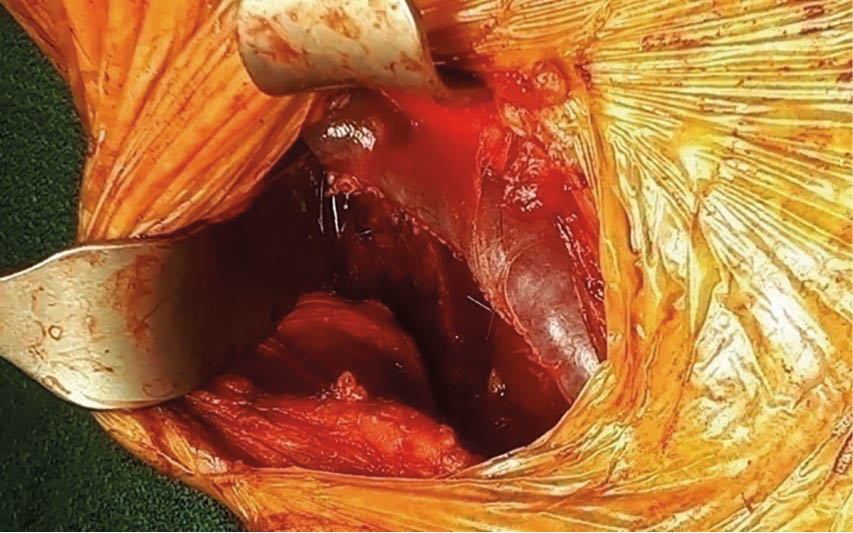
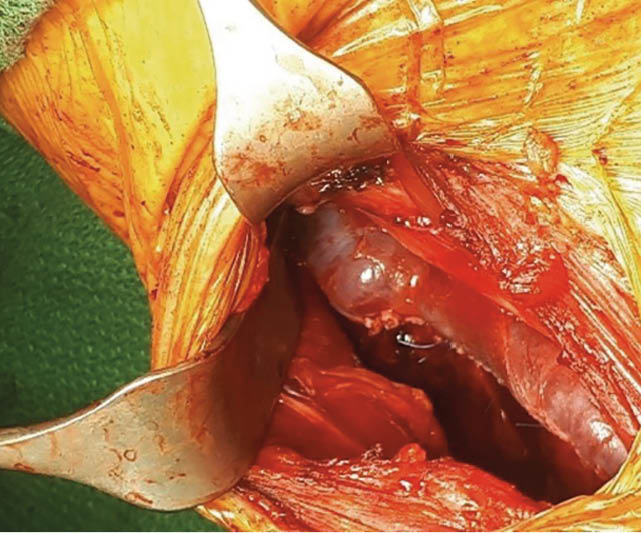
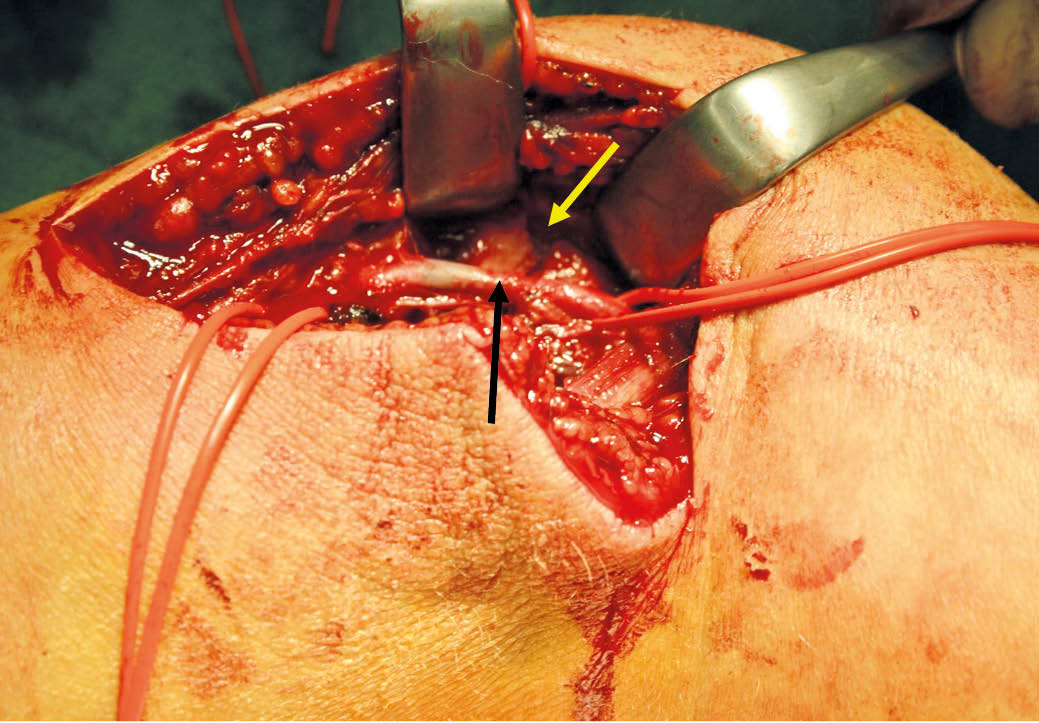
Unter diaphanoskopischer Kontrolle (Abb. 5) mussten die 2 weiteren epigastrischen Arbeitstrokare etwas mehr rechtsseitig positioniert werden. Intraoperativ (Abb. 6) stellte sich die Gallenblase sowohl akut als auch chronisch entzündlich verändert dar. Die Leber zeigte makroskopisch venöse Malformationen sowie einen beginnend kleinknotigen Parenchymumbau. Die laparoskopische Cholezystektomie verlief ohne Komplikationen, auf die Einlage von lokalem Drainagematerial konnte verzichtet werden. Die pathohistologische Aufarbeitung (Abb. 7) zeigte eine chronisch-fibrosierende Cholezystitis mit Gallenblasenwandverdickung ohne Anhalt für Malignität.
Die Patientin konnte am 3. postoperativen Tag bei subjektivem Wohlbefinden, reizlosen Wundverhältnissen und laborchemisch ausgeschlossener überschießender Gerinnungsaktivierung sowie stabilen Blutbildverhältnissen entlassen werden.
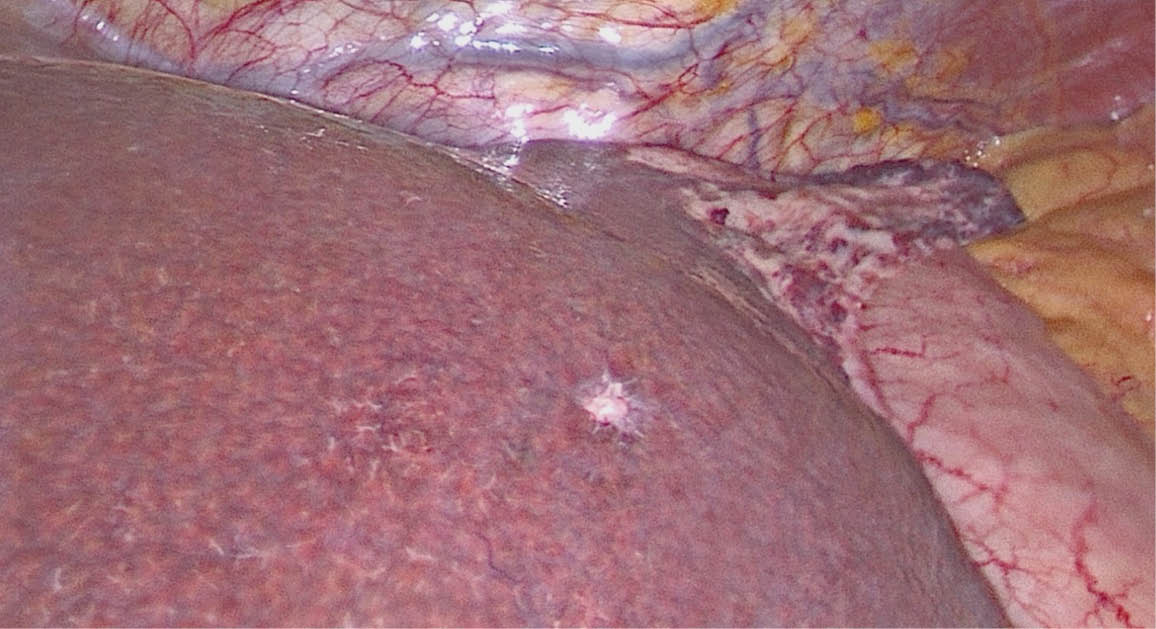
Abb. 5: Intraoperativer laparoskopischer Befund des Hämangioendothelioms der Rumpfwand linksseitig sowie auf dem Ligamentum triangulare sinistrum. Nebenbefundlich kleiner von-Meyenburg-Komplex im Lebersegment-II/III-Übergang bei Leberzirrhose
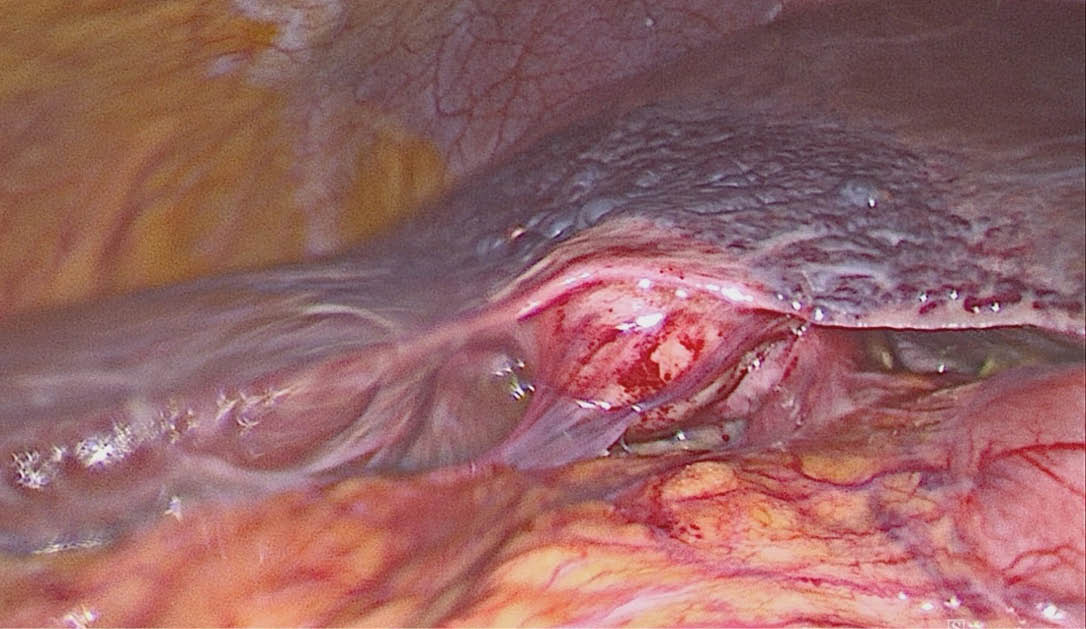
Abb. 6: Intraoperativer laparoskopischer Befund einer teils chronischen, teils akuten Cholezystitis sowie einer venösen Malformation der Leber (hepatisches Hämangiom) mit kleinknotigem Parenchymumbau i. S. einer Leberzirrhose
Das KMS ist durch die Kombination von (Riesen-)Hämangiomen an der Haut oder/und inneren Organen mit dem Potenzial für eine disseminierte intravasale Koagulation und Verbrauchskoagulopathie gekennzeichnet. Dabei wird eine genetische Ursache vermutet, die genaue Ursache ist jedoch nicht sicher bekannt. Überwiegend sind Frauen betroffen bei einer Prävalenz von 0,7/100.000 [2] (Mortalität: 30 % [3,4]). Das mediane Erkrankungsalter liegt bei 2 Monaten, selten manifestiert es sich erst bei Erwachsenen.
Die Symptomatologie ist von den bevorzugt über die gesamten Extremitäten verteilten Riesenhämangiome gekennzeichnet, insbesondere aber durch eine Blutungsneigung infolge eines Thrombozytenverbrauchs bei Verbrauchskoagulopathie bis hin zu einem drohenden Multiorganversagen.
Die Diagnosestellung ist nicht durch direkten Nachweis möglich (genaue Ursache unbekannt), die Symptomkombination gilt jedoch als einzigartig (kongenitale Hämangiome, Thrombozytopenie, dis-
seminierte intravasale Koagulopathie (DIC) möglich). In der Regel ist die Erkrankung nicht progredient, Spontanheilungen sind umstritten.
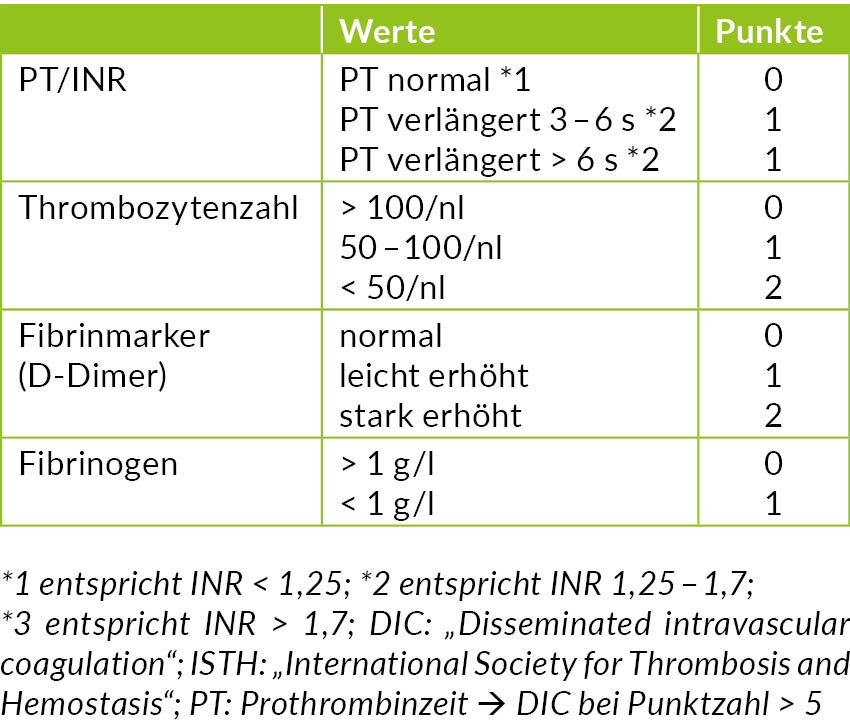
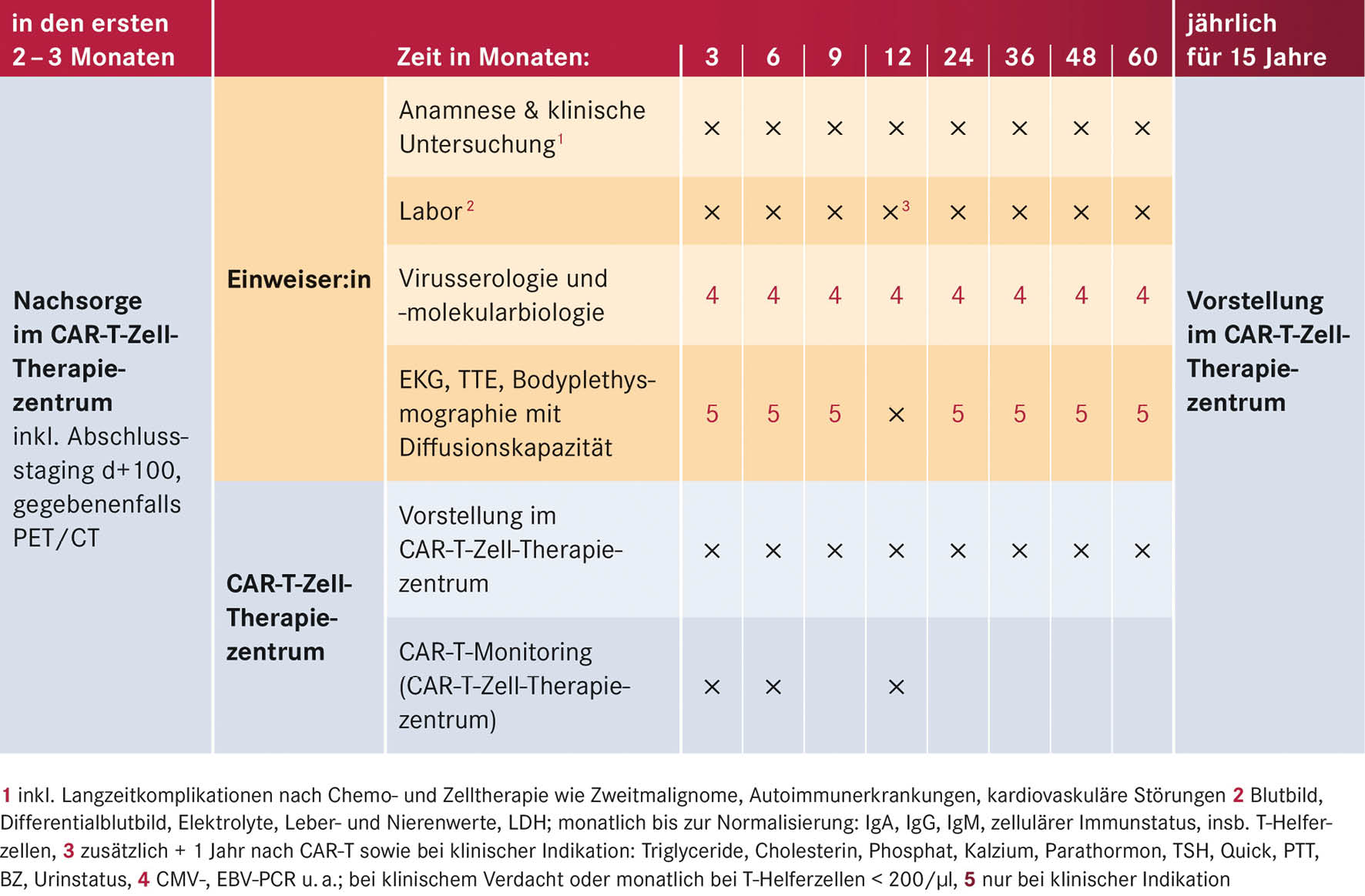
Tab. 1: Diagnostik des Kasabach-Merritt-Syndroms – mögliche Kriterien: DIC-Score der ISTH für die Diagnose einer manifesten disseminierten intravasalen Gerinnung
Das Therapiespektrum umfasst:
- laserchirurgische Entfernung,
- Embolisation (interventionelle Radiologie): Risiko lokaler Nekrosen, Tumore (Hämangiome) haben i. d. R. mehrere zuführende Gefäße,
- externe Kompression,
- α-Interferone und Kortikosteroide: lindern insbesondere die hohe Rezidivneigung,
- Propanolol – meist allein nicht ausreichend (oder)
- Substitution von Blutplättchen erst bei thrombozytopenischer Blutungsneigung.
Der Therapieerfolg wird an der Wiederherstellung der Hämostase und der Elimination von Tumorzellen gemessen, wobei der frühe definitive chirurgische Behandlungserfolg des KMS in einer höheren Heilungsrate und reduzierten Medikamentennebenwirkungen resultiert. Die Histologie zeigt ein lokal aggressives, dabei stark variierendes Zellwachstum, wobei mehrere Gewebsschichten involviert sind (demgegenüber ist beim „normalen“ Hämangiom nur eine Schicht betroffen). Beide Entitäten sind positiv für die Bio-Marker:
- D2-40 (Podoplanin Antikörper),
- LYVE1 (Lymphatic Vessel Endothelial Hyaluronan Receptor 1)
- Prox-1 (Prospero Homeobox Protein 1), jedoch negativ für GLUT-1 (Protein für Glukosetransport).
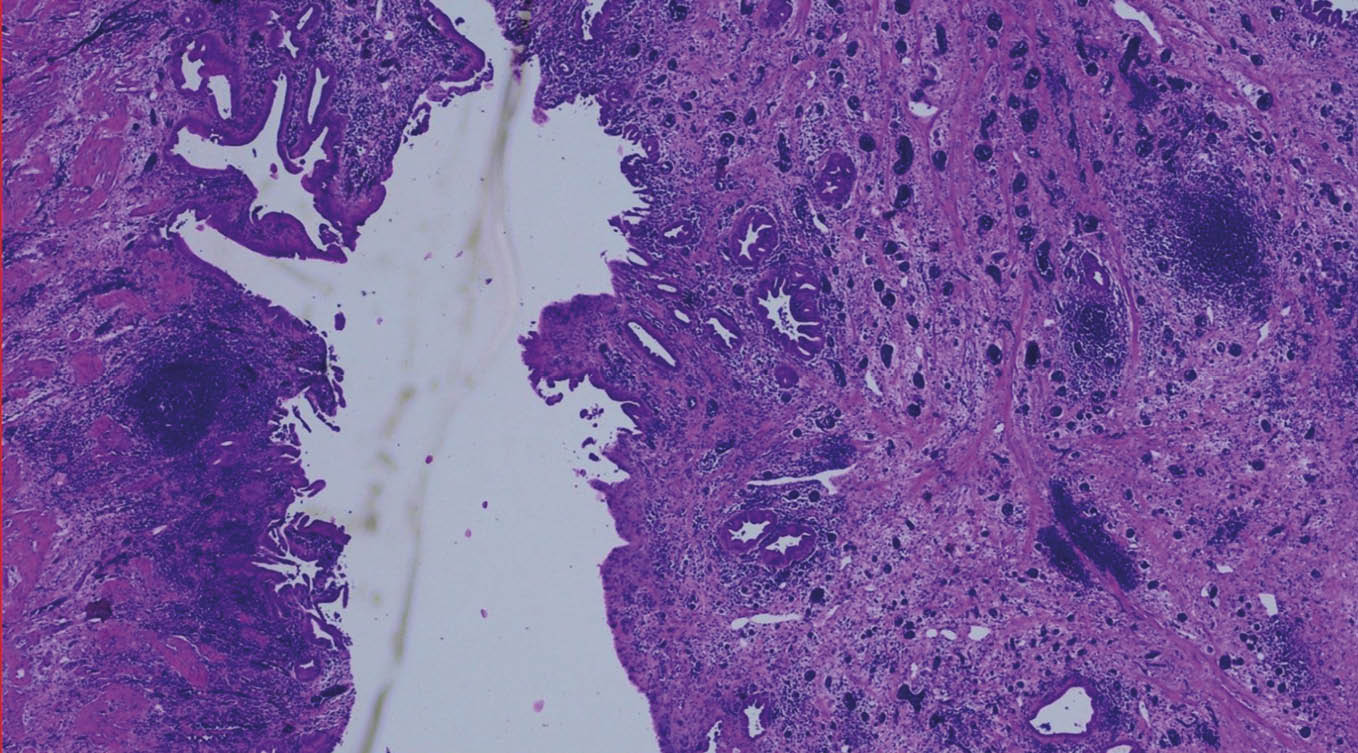
Abb. 7: Lupenvergrößerung (2 x objektiv = Vergrößerung x 20) des Gallenblasenfundus. Bereits in der Übersicht auffällig: Op-bedingt Blut-gestaute Gefäße (1) und chronisches Entzündungsinfiltrat (2)
Hauthämangiome weisen eine Mortalität von 10 % auf, retroperitoneale Tumore hingegen je nach Angabe von bis zu 60 %. Beachtenswert ist dabei die Tatsache, dass diese Lokalisation nicht selten bei der körperlichen Untersuchung übersehen werden kann bei teils nur milden abdominellen Beschwerden, was die durchschnittliche Mortalität von 30 % ansteigen lässt. Differenzialdiagnostisch abzugrenzen sind Hämangiome, die bei 3 – 5 % der Säuglinge vorkommen und einen embryonalen „Tumor“ mit Endothel-Proliferation bei sekundärer Ausbildung von Gefäßlumina darstellen. 80 % der Hämangiome bilden sich bis zum 5. Lebensjahr zurück. Histologisch sind blutgefüllte, weite Gefäße mit flacher Endothelauskleidung charakteristisch, kleinere Hämangiome sind auch mit Propanolol behandelbar.
Der vorgestellte Fall veranschaulicht in repräsentativer Weise die beachtenswerten Aspekte bei chirurgischer Indikationsstellung zur Operation: Bei anstehender operativer Versorgung ist der Eingriff sorgfältig zu planen (insbesondere unter elektiven Kautelen) hinsichtlich der Hämangiomausdehnung und der Tangierung des potenziellen Op-Feldes bzw. einer Prüfung von Alternativoptionen des Vorgehens (Zugangslokalisation, offen/laparoskopisch etc.), um intra-/postoperativ Blutungskomplikationen bestmöglich für die Wahrung einer hohen Patientensicherheit zu vermeiden. Als Limitation ist die lediglich singuläre Erfahrung zum perioperativen Management anzuführen.
Chirurgisch zu versorgende Krankheitsbilder bei koinzidentellem KMS erfordern eine enge Zusammenarbeit mit einem Hämostaseologen sowie eine entsprechende prä- und perioperative Gerinnungsdiagnostik. Eine blutarme Versorgung unter perioperativer Thromboseprophylaxe und medikamentöser Hyperfibrinolysehemmung (Tranexamsäure) verhindert die Aktivierung des Gerinnungssystems und den Verbrauch von Gerinnungsfaktoren. Auch eine Thrombozytentransfusion sollte aufgrund einer Gerinnungsaktivierung vermieden werden [5].
Insbesondere unter elektiven Kautelen ist die Hämangiomausdehnung mit möglicher Tangierung des potenziellen Op-Feldes sorgfältig abzuklären (Sonographie, Angio-CT, MRT), um hieraus Modifikationen des Vorgehens (Zugangslokalisation, offen/laparoskopisch etc.) abzuleiten.
An
- koinzidientielle Herzinsuffizienz infolge hoher Shuntvolumina,
- das Vorliegen einer Cirrhose cardiaque (und)
- Infektionskrankheiten, hervorgerufen durch stattgehabte Massentransfusionen,
sollte bei der Planung einer elektiven chirurgischen Versorgung gedacht werden.
Foto: Universitätsklinikum Magdeburg A. ö. R.
Korrespondenzanschrift:
Dr. Stephan Arndt
Klinik für Allgemein-, Viszeral-, Gefäß- und Transplantationschirurgie
Arbeitsbereich Gefäßchirurgie
Universitätsklinikum Magdeburg A. ö. R.
Leipziger Straße 44
39120 Magdeburg
Tel.: 0391/671 56 93
Fax: 0391/671 55 41
E-Mail:
- Kasabach HH, Merritt KK. Capillaryhaemangioma with extensive purpura. Am J Dis Child 1940;59:1063
- Croteau SE, Liang MG, Kozakewich HP, Alomari AI, Fishman SJ, Mulliken JB, Trenor CC. Kaposiform hemangioendothelioma: atypical features and risks of Kasabach-Merritt phenomenon in 107 referrals. J Pediatr 2013;162(1):142-7
- Putra J, Gupta A. Kaposiform haemangioendothelioma: a review with emphasis on histological differential diagnosis. Pathology 2017;49(4):356-62
- Mahajan P, Margolin J, Iacobas I. Kasabach-Merritt Phenomenon: Classic Presentation and Management Options. Clin Med Insights Blood Disord 2017;10:1179545X17699849
Weitere Artikel
Weiterlesen … Fachbeitrag 05/2024 - Kasabach-Merritt-Syndrom
- Aufrufe: 5059