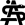Konservative Therapie
An erster Stelle der Arthrosetherapie stehen die konservativen Therapieoptionen. Im Rahmen der Physiotherapie sollte der Schwerpunkt in der manualtherapeutischen Mobilisation des Gelenkes liegen sowie die funktionelle Korrektur der Beinachse erfolgen. Wesentliche Aufgabe ist es dabei, eine ausreichende Compliance des Patienten zu erreichen. Hierfür ist eine angemessene Aufklärung und die Vermittlung eines Eigenübungsprogramms notwendig. Gegebenenfalls kann im Akutstadium eine temporäre Entlastung, eine analgetisch-antiphlogistische Therapie oder eine Injektionstherapie erfolgen. Durch Orthesen oder Einlagen können Fehlstellungen oder Bandinstabilitäten symptomorientiert behandelt werden, ohne die zugrundeliegende Ursache zu beheben. Insbesondere bei beginnender Arthrose ist die Versorgung mit orthopädischen Hilfsmitteln als Therapieoption zu beachten (9).
Umstellungsosteotomie
Bei asymmetrischer OSG-Arthrose kann durch Umstellungsosteotomien, besonders in frühen Arthrosestadien, das Fortschreiten aufgehalten oder zumindest relevant verzögert werden (10).
Der überwiegende Teil der Fehlstellungen liegt in der coronaren Ebene. Am häufigsten liegt eine Varusdeformität vor, welche sich bei lateraler Bandinsuffizienz entwickelt (11). Eine supramalleolare Osteotomie, welche auf die Druckumverteilung im OSG abzielt, kann als gelenkerhaltende Strategie insbesondere bei jüngeren Patienten sinnvoll sein. Abhängig von der Ausgangssituation kann eine Osteotomie der distalen Fibula notwendig werden. Besteht eine Valgusdeformität, wird mit der supramalleolaren Umstellung eine Varisierung der Druckverteilung in der Gelenklinie erreicht. Sowohl lateral-aufklappende (open-wedge) als auch medial-zuklappende (closed-wedge) sowie Dome-Osteotomien finden Anwendung (12, 13). Bei kombinierten Deformitäten der Rückfußachse ist die Calcaneus-Osteotomie in Betracht zu ziehen (14). Neben der knöchernen Korrektur müssen gleichzeitig auch mögliche ligamentäre Instabilitäten adressiert werden. Bei erfolgten Korrekturen in frühen Arthrosestadien (Stadium I,II) zeigen sich zufriedenstellende Ergebnisse. Ab Stadium III spricht man von einer endgradigen Arthrose, welche für eine Therapie mittels alleiniger Umstellungsosteotomie nicht mehr in Frage kommt (2). Bei ca. 25 % sind nach stattgehabter supramalleolärer Umstellung auf Grund einer voranschreitenden Arthrose oder fortbestehenden klinischen Symptomatik weitere operative Versorgungen mittels Prothesenimplantation oder Arthrodese notwendig (12, 15).
Endoprothese
Ansätze das OSG endoprothetisch zu versorgen, erfolgten bereits zu Beginn der 1970er Jahre. Der erste Versuch eines Gelenkersatzes wurde von Lord und Marotte durchgeführt, indem sie einen invertierten Hüftschaft in der Tibia und eine Gelenkpfanne am Calcaneus implantierten (16).
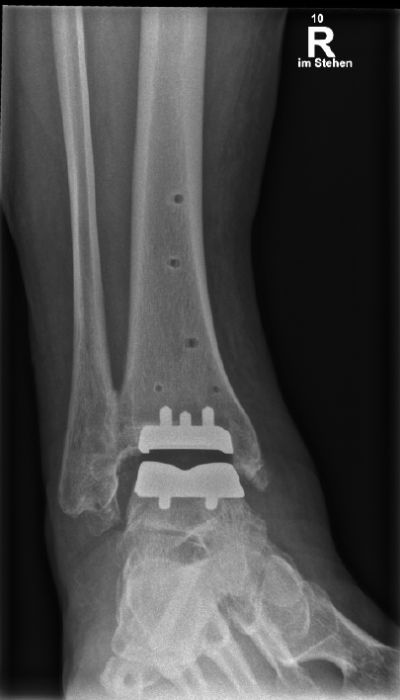
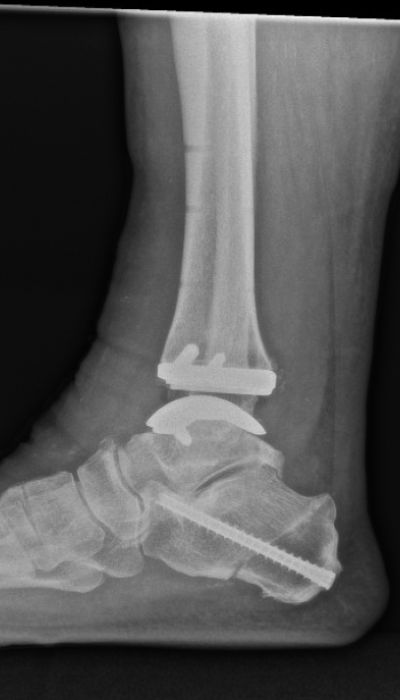
Seitdem ist eine umfangreiche technische Entwicklung des Designs, der Implantatbeschichtung und der Implantationstechnik vollzogen worden (17-19). Lange hatte die Endoprothetik des OSG mit kurzen Standzeiten und Komplikationen zu kämpfen. Die heute zur Verfügung stehenden Konzepte kommen den Standzeiten der Hüft- und Knieendoprothesen immer näher (20). Während früher Fehlstellungen im OSG als Ausschlusskriterium betrachtet wurden, erfolgt heute die Achskorrektur durch Osteotomie ein- oder zweizeitig im Rahmen der Implantation der Endoprothese (Abbildung c,d). Wichtig ist die sorgfältige Behandlung von Inkongruenzen im Sprunggelenk mit Wiederherstellung des korrekten Alignments. Wird die Fehlstellung regelrecht behoben, sind die biomechanischen Resultate vergleichbar mit denen ohne vorbestehende Inkongruenz (21). Studien konnten zeigen, dass bei Varus-Fehlstellung bis zu 30° präoperativ nach Prothesen-Implantation mit erfolgtem Re-Alignment kein relevanter Unterschied im funktionellen Outcome zu betrachten ist (22).
Die vorhanden Revisionslösungen ermöglichen die Versorgung auch von jüngeren Patienten. Die in der Vergangenheit bei jüngeren Patienten oft favorisierte Versorgung mit OSG-Arthrodese erscheint unter Berücksichtigung der zu erwartenden Anschlussarthrosen des unteren Sprunggelenkes und der Fußwurzel als keine universelle moderne Versorgungsoption. Die Auswertung eigener Ergebnisse nach OSG-TEP-Versorgung der Patienten aus dem Hämophiliezentrum mit einem durchschnittlichen Alter von 28 Jahren (n=12) zeigte bei sorgfältiger Patientenselektion und -aufklärung keine relevanten Unterschiede in der Komplikations- bzw. Revisionsrate gegenüber Patienten ohne Blutgerinnungsstörung. Viel mehr lassen sich durch den Erhalt der Beweglichkeit des OSG positivere Langzeitverläufe erhoffen.
Die neueren Registerdaten spiegeln die positive Entwicklung der OSG-Endoprothetik wider und lassen diese als eine sichere und reproduzierbare Behandlungsstrategie erscheinen (23). Durch moderne Versorgungskonzepte mit simultaner oder zweizeitiger Korrektur der Begleitdeformitäten lassen sich auch schwere Rückfußdeformitäten balancieren. Insbesondere die Kombination mit minimal-invasiven Techniken senkt die Gesamtmorbidität des Eingriffes erheblich (24). Sind keine zusätzlichen Umstellungsosteotomien und korrigierenden Arthrodesen des Rückfußes notwendig, so ist mit den modernen OSG-Endoprothesen eine rasche postoperative Belastungsaufnahme, meistens nach Wundheilung, möglich (25). Die durchschnittliche Beweglichkeit nach Implantation einer OSG-TEP wird in der Literatur mit 25 – 38° in der Sagittalebene beschrieben (26, 27). Insbesondere bei präoperativ stark eingeschränkter Beweglichkeit lässt sich durch die Implantation der Prothese eine Verbesserung des Bewegungsausmaßes erzielen (28). Eines der zentralen Argumente für die OSG-Prothese stellt neben dem Erhalt der OSG Funktion auch die Schonung der Nachbargelenke dar. Eine Reihe von Arbeiten hat die problematische Entwicklung von Anschlussarthrosen nach OSG-Arthrodese nach bereits 10 Jahren aufgezeigt (29, 30). Vor allem Patienten mit bereits bestehender Arthrose des unteren Sprunggelenks (USG) oder aber nach bereits durchgeführter Arthrodese des USG-Komplexes profitieren von einem beweglichen OSG, welches die Versorgung mit einer OSG-Endoprothese gewährleistet. Im Gegensatz dazu sind insbesondere in diesen Fällen unzufriedenstellende Ergebnisse durch OSG-Arthrodese zu erwarten. Im Fokus der aktuellen Forschung bleibt die Thematik der Zystenbildung. Multifaktorielle Ursachen wie Abrieb, Stress-„shielding“ und Micromotion scheinen die zentrale Rolle zu spielen (31). Auch die Ergebnisse nach Versorgung mit „fixed-bearing“ und „mobile-bearing“ Komponenten erfordern eine weitere detaillierte Betrachtung.
Fallbericht
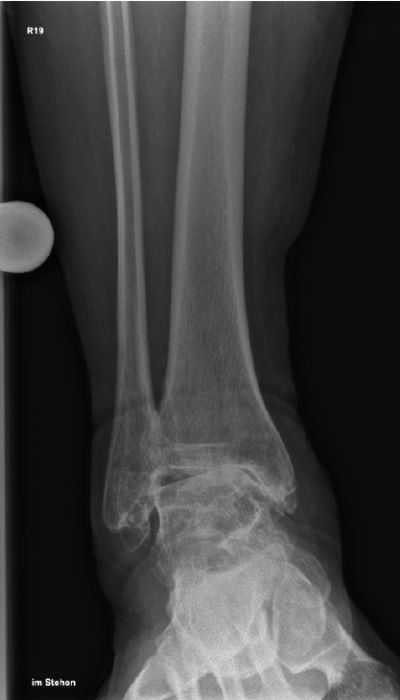
Der Patient, 78 J., männlich, stellte sich mit seit Jahren bestehenden, progredienten Schmerzen im rechten OSG in der Sprechstunde vor. Klinisch zeigte sich eine plantigrade Fußstellung bei varischer Rückfußachse. Die Beweglichkeit war eingeschränkt, Dorsal-/Plantarflexion OSG rechts 0/0/35°. Motorik, Durchblutung und Sensibilität waren intakt. Im Röntgen wurde eine viertgradige OSG-Arthrose bei ausgeprägter varischer Verkippung des Talus und Synostose des distalen Tibiofibulargelenkes deutlich. Nach Ausschöpfung der konservativen Therapiemaßnahmen stellten wir die Indikation zur Implantation einer OSG-TEP mit ergänzender minimalinvasiver Umstellungsosteotomie des Calcaneus. Postoperativ erfolgte die Mobilisation im langen Walker mit Bodenkontaktlauf. 6 Wochen postoperativ lagen reizlose Narbenverhältnisse vor. Das Bewegungsausmaß stellte sich mit Dorsal-/Plantarflexion 10°/0°/40° verbessert dar. Es bestand noch eine moderate Schwellneigung. Im Röntgen zeigte sich eine gut integrierte OSG-Endoprothese bei unveränderter Implantatlage und knöchern fusionierter Calcaneus-Osteotomie. Von Seiten des Patienten bestand eine deutliche Reduktion der Schmerzen und subjektive Zufriedenheit. Anschließend erfolgte eine rasche Steigerung der Belastung bis zur Vollbelastung ohne Walker und Gehstützen.
Arthrodese
Bei bestehender Kontraindikation zur Implantation einer OSG-Endoprothese z. B. bei erheblicher infektassoziierter Destruktion, schlecht eingestelltem Diabetes mit Polyneuropathie oder bei neurologischen Störungen bleibt die Arthrodese als „Salvage Procedere“ erhalten (25).
Für die Arthrodese des OSG stehen diverse operative Vorgehensweisen zur Verfügung. Sowohl eine isolierte tibiotalare Arthrodese bei erhaltenem Subtalargelenk als auch tibio-talo-calcaneare Arthrodese-Verfahren bei arthrotischem Subtalargelenk finden ihre Anwendung. Je nach geplanter Arthrodese wird ein Verfahren durch Schrauben, Platten, einen Nagel oder Ringfixateur (vor allem in Infektsituationen und in der Behandlung der Charcot-Arthropathie) gewählt. Es stehen offene und arthroskopische Operationstechniken zur Verfügung (32). Bei isolierter OSG-Arthrodese zeigen arthroskopische Verfahren in der aktuellen Literatur geringere Wundheilungsstörungen und eine höhere Durchbauungsrate (33). In klinischen und biomechanischen Studien des eigenen Zentrums konnte die Überlegenheit der posterolateralen Plattenarthrodese gegenüber der Schraubenarthrodese bzw. der Nagelarthrodese in Bezug auf die Fusionsrate bzw. Stabilität aufgezeigt werden (34). Bei geplanten offenen Arthrodesen in Fällen mit erheblicher rigider Deformität ist die posterolaterale Plattenarthrodese ein häufig favorisiertes Verfahren (35).
Eine Pseudarthrosenrate von 1,1 % bis 41 % wird in der aktuellen Literatur unabhängig vom Osteosyntheseverfahren angegeben, wobei die höheren Raten an Pseudarthrosen bzw. Komplikationen vor allem den Risikogruppen zuzuschreiben sind (36-38). Patienten mit Diabetes, Polyneuropathie, Charco-Arthropathie und septischer Arthritis gehören im hohen Maß zu der entsprechenden Risikogruppe. In unserem Zentrum werden diese Risikopatienten überwiegend mit einem Taylor-Spatial-Frame (TSF) bzw. einer kombinierten Versorgung mit TSF und interner Osteosynthese versorgt. Eine erhebliche Reduktion der Komplikationsrate konnte in der eigenen vergleichenden Studie durch die Kombination der arthroskopischen OSG-Arthrodese und TSF demonstriert werden (39). Die genaue Analyse der vorhandenen Deformität und des bestehenden Risikoprofils des Patienten bestimmen maßgeblich die optimale Herangehensweise unter Berücksichtigung der zur Verfügung stehenden operativen (offen vs. arthroskopisch) und osteosynthetischen Verfahren (37). Außerhalb der Risikogruppen unter gleichzeitiger Berücksichtigung der langfristigen Folgen der OSG-Arthrodese wie Anschlussarthro-sen (40), sieht man die Indikationszahlen für die OSG-Arthrodese deutlich zu Gunsten der endoprothetischen Versorgung zurückgehen.
Limitationen des Artikels
Dieser Artikel soll eine Übersicht zur Behandlung der Arthrose im OSG bieten. Die Bewertung und Einordnung der Behandlungsstrategien sind dazu auf aktuelle Studien und Studien der vergangenen Jahre gestützt. Generell liegt in der Darstellung des „Status quo“ die Gefahr, dass diese nur für einen begrenzten Zeitraum eine adäquate Bewertung der Studienlage bietet. Durch neue Entwicklungen, weitere wissenschaftliche Arbeiten kann und muss eventuell die Einordnung der Thematik zu einem späteren Zeitpunkt anders ausfallen. Des Weiteren ist dieser Übersichtsartikel auf einer freien Rechereche basierend und somit kein systematisches Review. Dadurch kann nicht ausgeschlossen werden, dass gegebenenfalls relevante Publikationen nicht erwähnt wurden.
Ausblick
In diesem Artikel wird dargestellt, dass es einen Wandel der operativen Versorgung der fortgeschrittenen OSG-Arthrose gibt. In der Medizin lassen sich auf vielen Gebieten langfristige Entwicklungen und die Ausbildung neuer Paradigmen beobachten. Auf der anderen Seite gibt es jedoch auch Trends von weniger Nachhaltigkeit. Somit wird es spannend zu sehen sein, ob die Endoprothetik am OSG die Entwicklungen mit steigenden Versorgungszahlen, gebesserten klinischen Ergebnissen und zunehmenden Standzeiten fortsetzen kann. Hierzu werden insbesondere Langzeitstudien und die Auswertung von Registerdaten von Interesse sein. Parallel dazu spielt in der Endoprothetik des OSG die technische Entwicklung eine bedeutende Rolle. Hier wird zu beobachten sein, ob neue Materialien oder Prothesenmodelle einen weiteren positiven Anstoß geben können. Sowohl in Hinblick auf Nutzungsdauer und Funktion, aber auch in Hinblick auf die aktuellen Komplikationen (s.o.) die mit OSG-TEPs einhergehen können.