Fachbeitrag 06/2025 - Kurative Behandlung von Hämoglobinopathien in Sachsen-Anhalt
- Titel Fachbeitrag: Kurative Behandlung von Hämoglobinopathien in Sachsen-Anhalt
- Ärzteblatt Ausgabe: ÄB 2025/06
- Autor: Kinan Kafa
Kurative Behandlung von Hämoglobinopathien in Sachsen-Anhalt
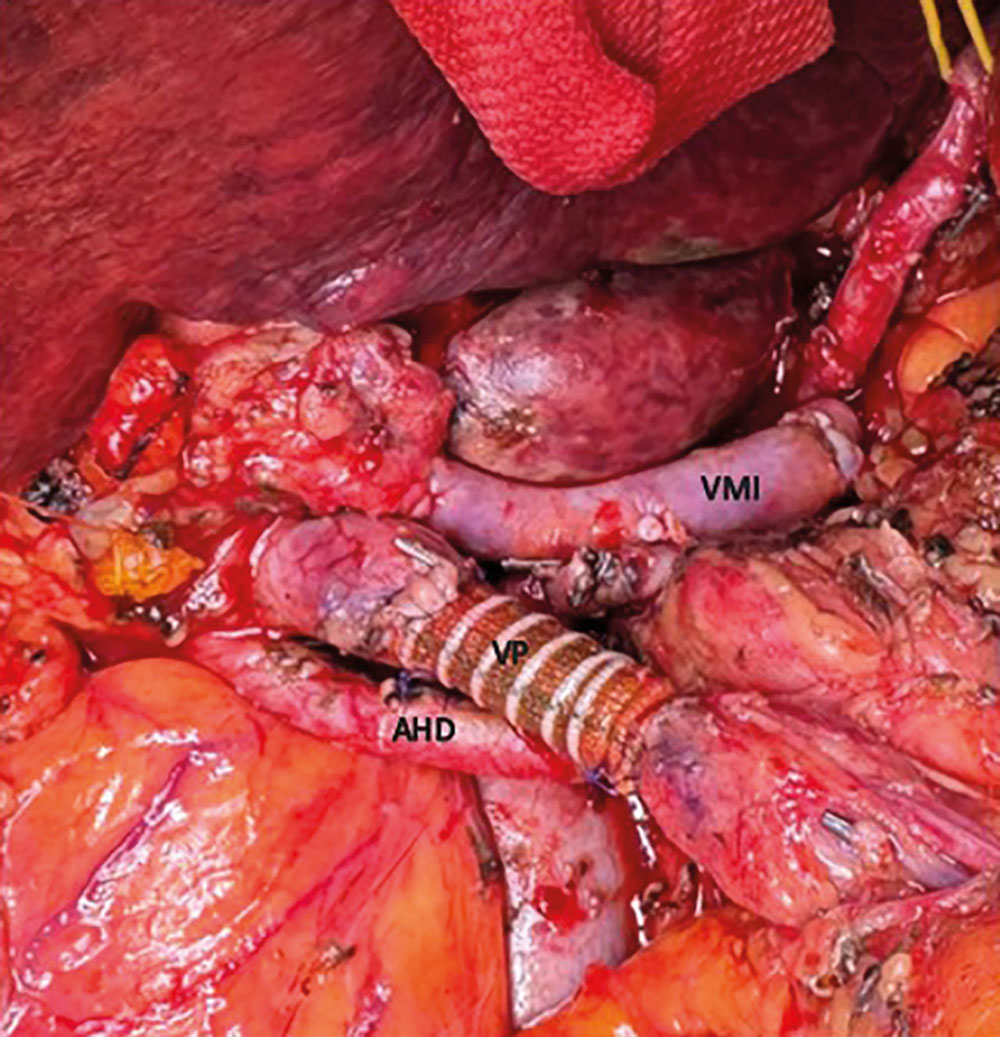
Fotos: Universitätsmedizin Halle | kryokonservierte gentechnisch veränderte Zellen
E. Knorr1, L. Lessel2, S. Hettmer1, L. P. Müller3 und K. Kafa1
1 Universitätsklinik und Poliklinik für Pädiatrie I der Universitätsmedizin Halle
2 Pädiatrische Hämatologie und Onkologie der Universitätskinderklinik der Universitätsmedizin Magdeburg
3 Universitätsklinik und Poliklinik für Innere Medizin IV der Universitätsmedizin Halle

E. Knorr1, L. Lessel2, S. Hettmer1, L. P. Müller3 und K. Kafa1
1 Universitätsklinik und Poliklinik für Pädiatrie I der Universitätsmedizin Halle
2 Pädiatrische Hämatologie und Onkologie der Universitätskinderklinik der Universitätsmedizin Magdeburg
3 Universitätsklinik und Poliklinik für Innere Medizin IV der Universitätsmedizin Halle

Repräsentative Kasuistik
Ein 15-jähriger Jugendlicher kommt alle drei Wochen auf die Tagesstation des Universitätsklinikums Halle (Saale), um eine Bluttransfusion zu erhalten. Er hat eine homozygote Beta-Thalassämie. Trotz täglicher Einnahme eines Eisenchelatbildners sind – ohne zusätzliche Maßnahmen – eine Eisenüberladung und, damit verbunden, Leberfunktionsstörungen, eine Herzinsuffizienz und endokrine Ausfälle im jungen bis mittleren Erwachsenenalter vorprogrammiert. Der Junge hat kein HLA-identisches, gesundes Geschwister, aber die Fremdspendersuche identifiziert eine/n an 10 von 10 HLA-Genorten passende/n Fremdspender/in.
Familie und Behandlungsteam entscheiden sich gemeinsam für eine hämatopoetische Stammzelltransplantation (HSZT). Im Verlauf der Transplantation kommt es – bedingt durch die myeloablative Konditionierung – zu Mukositis und Fieber in Neutropenie sowie zu einer akuten „Graft-versus-Host“-Reaktion der Haut, welche mit Prednisolon erfolgreich behandelt wird. Infolge der Immunsuppression tritt während der Nachsorge eine Herpes simplex Virus-Reaktivierung mit Stomatitis auf, welche für einige Tage mit einer intravenösen systemischen Aciclovirtherapie behandelt werden muss. Kurzzeitig ist eine teilparenterale Ernährung notwendig. Doch die Transplantation ist erfolgreich. Der Patient hat einen vollständigen Chimärismus und seit über 12 Monaten keinen Transfusionsbedarf. Zur Therapie der vorbestehenden sekundären Eisenüberladung und zur Prävention von Organschäden erhält er im Abstand von 3 bis 4 Wochen noch Aderlässe. Er besucht die 8. Klasse und macht gute Fortschritte. In absehbarer Zukunft wird er keine Aderlässe oder Medikamente mehr brauchen.
Einleitung
Hämoglobinopathien sind die am weitesten verbreiteten monogenetischen Erkrankungen und betreffen mehrere Millionen Menschen weltweit. Unter diesen stellen Thalassämien und die Sichelzellkrankheit (SCD) die häufigsten Krankheitsbilder dar. Trotz eines rückläufigen Trends bei der Häufigkeit der Diagnosen von Hämoglobinopathien bei Neugeborenen bleibt diese Erkrankung in zahlreichen Ländern ein bedeutendes gesundheitliches Problem. Regelmäßige Erythrozytentransfusionen, Fortschritte in der Eisenchelation sowie unterstützende therapeutische Maßnahmen haben zu einer Verbesserung der Lebenserwartung beigetragen.
Dennoch ist bisher die allogene hämatopoetische Stammzelltransplantation (HSZT) die einzig kurative Option für Patientinnen und Patienten mit Hämo-globinopathien, um irreversible Organschäden zu verhindern. Die jüngsten Fortschritte im Bereich der Transplantationsmedizin und die verbesserte Nachsorge der Patientinnen und Patienten nach der Transplantation haben signifikant zur Erhöhung der Überlebensraten beigetragen. Daneben werden gentherapeutische Ansätze die Therapiekonzepte in Zukunft verändern.
Ziel des Beitrags ist es, den niedergelassenen Ärztinnen und Ärzten in Sachsen-Anhalt einen strukturierten Überblick über die aktuelle Versorgungssituation von Patientinnen und Patienten mit Hämoglobinopathien zu geben. Dabei sollen das bestehende Versorgungskonzept an den beiden universitären Standorten in Magdeburg und Halle (Saale) vorgestellt sowie deren koordinierende Rolle im Versorgungspfad verdeutlicht werden.
Thalassämien: Definition, Epidemiologie und natürlicher Verlauf
Thalassämien sind genetisch bedingte Störungen der Hämoglobinproduktion, die durch eine verminderte oder fehlende Synthese der alpha- oder Beta-Globinketten des Hämoglobins verursacht werden. In der Folge kommt es kompensatorisch zu einer übermäßigen Bildung der anderen Globine, welche durch Präzipitation einen Zellzerfall schon während der Erythropoese auslösen. Die Anämie induziert eine vermehrte Erythropoietin (EPO)-Ausschüttung, welche die ineffektive Erythropoese weiter stimuliert (circulus vitiosus) und zur gesteigerten intestinalen Eisenrückresorption mit nachfolgender Eisenüberladung führt. Je nach Anzahl und Art der betroffenen Gene ergeben sich erhebliche Unterschiede im klinischen Verlauf. Bei der Beta-Thalassämie major zeigt sich eine schwere mikrozytäre Anämie mit hämolytischer Komponente und eine Hepatosplenomegalie. Bei unzureichender Therapie entstehen Knochendeformitäten mit Osteoporose, eine Facies thalassaemica und Wachstumsretardierung sowie durch Eisenüberladung bedingte Schäden vor allem an Herz und endokrinen Organen.
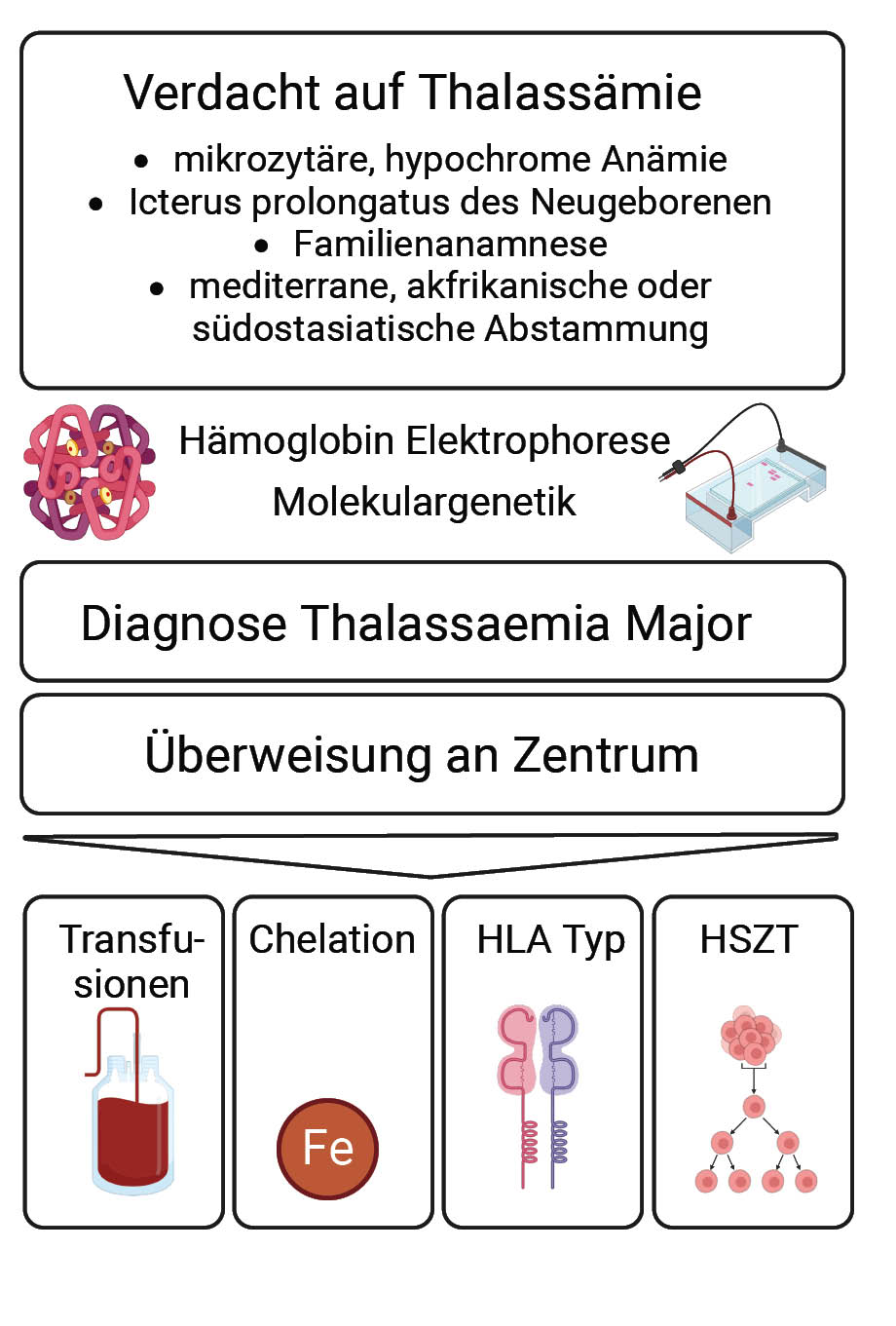
Weit verbreitet sind Thalassämien aufgrund des Selektionsvorteils in den Malariagebieten Afrikas, Südostasiens und Indiens; sie treten zudem gehäuft im mittleren Osten und Mittelmeerraum auf. In Deutschland sind ca. 400.000 Menschen Trägerinnen und Träger einer der Thalassämie-verursachenden Genvarianten. Mit optimaler Therapie in Form von Transfusionen von Erythrozytenkonzentraten und Einnahme von Eisenchelatbildnern sowie supportiver Therapie bei Organkomplikationen können Patientinnen und Patienten mit Beta-Thalassämie major in Industrienationen inzwischen bis zu 50 bis 60 Jahre alt werden. Viele Todesfälle treten dennoch bereits vor dem 40. Lebensjahr auf. Unbehandelt versterben Kinder mit Beta-Thalassämie major in den ersten Lebensjahren (1-4).
Sichelzellanämie: Definition, Epidemiologie und natürlicher Verlauf
Die Sichelzellkrankheit fasst genetisch bedingte Erkrankungen zusammen, welche durch die Bildung von Hämoglobin S (HbS) entstehen. Die Erkrankung führt dazu, dass rote Blutkörperchen eine sichelartige Form annehmen, was ihre Flexibilität und Fähigkeit zum Sauerstofftransport beeinträchtigt. Die Sichelzellkrankheit tritt vor allem in Afrika, Teilen Indiens und im östlichen Mittelmeerraum auf. Diese Verbreitung ist auf den Selektionsvorteil zurückzuführen, den das HbS-Allel bei Malaria-Infektionen bietet. Die Vererbung erfolgt autosomal-kodominant. In Deutschland liegt die Inzidenz bei etwa 100 bis 150 Neugeborenen pro Jahr, während weltweit zwischen 300.000 und 400.000 Neugeborene jährlich betroffen sind (5; 6).
Die Sichelzellkrankheit ist definiert durch einen HbS-Anteil am Gesamthämoglobin von über 50 %. Die wichtigsten Unterformen sind die homozygote Sichelzellkrankheit (SCD-S/S), die HbSC-Krankheit (SCD-S/C) und die Sichelzell-Beta-Thalassämie. Die Ausprägung der Symptomatik unterscheidet sich je nach Unterform; der Überträgerstatus weist normalerweise keinen Krankheitswert auf (7).
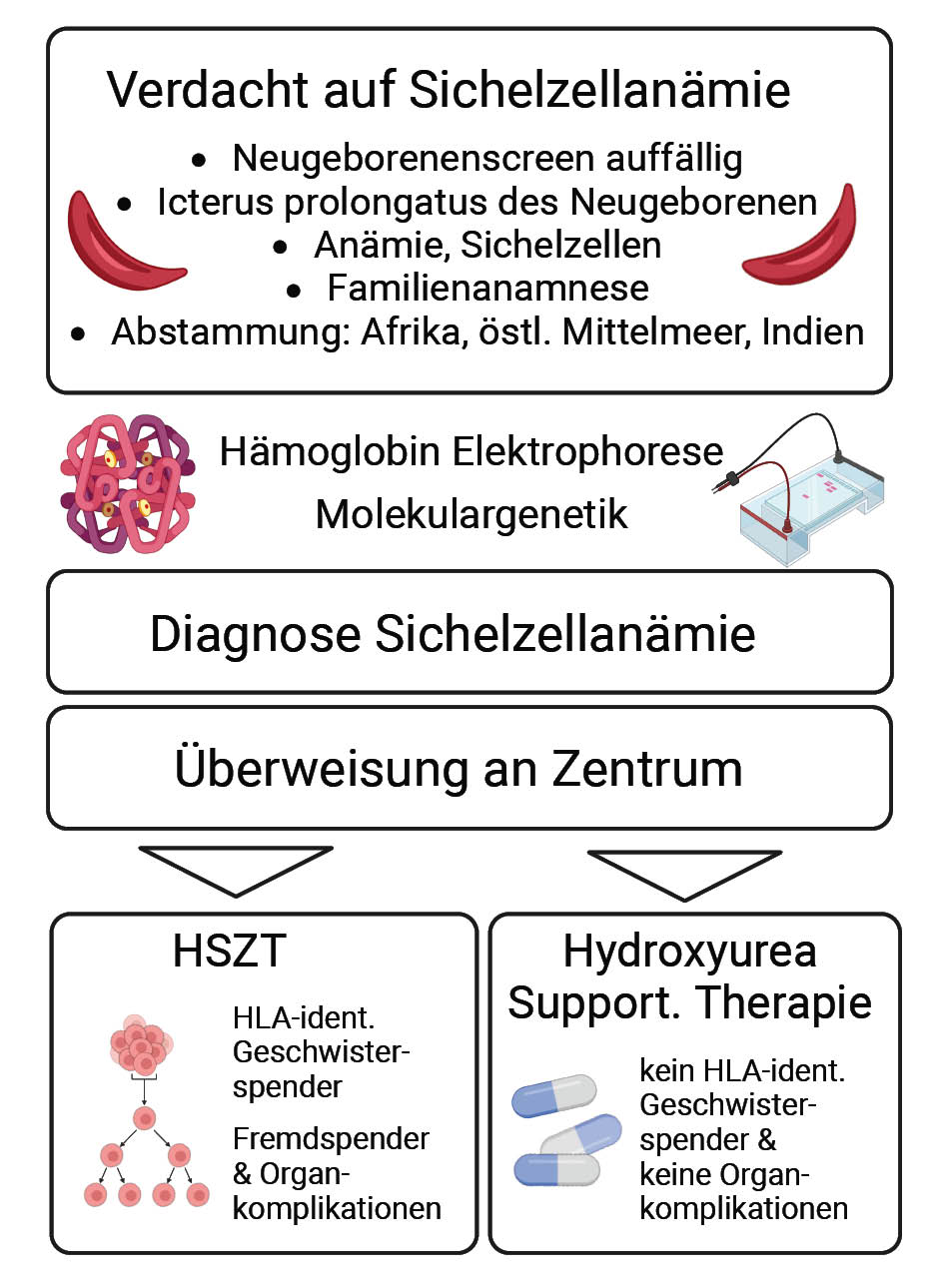
Der ursächliche Gendefekt ist eine Punktmutation, welche zu einer defekten Beta-Kette und dadurch zur Bildung von veränderten Hämoglobinmolekülen (HbS) führt, die das normale Hämoglobin (HbA) ersetzen, was zu einer chronischen hämolytischen Anämie, Endothelschäden und wiederkehrenden Gefäßokklusionen mit Schmerzkrisen und Organinfarkten mit nachfolgender Funktionseinschränkung führt. Bereits früh entsteht eine funktionelle Asplenie und damit eine erhöhte Infektionsneigung. Trotz Früherkennung durch Neugeborenenscreening, zeitiger und adäquater Therapie (insbesondere Penicillinprophylaxe und Hydroxycarbamid zur Steigerung des HbF-Anteils) sowie regelmäßiger Transfusionen beträgt die Lebenserwartung für Patientinnen und Patienten mit homozygoter Sichelzellkrankheit in den USA und Europa etwa 40 bis 50 Jahre. Erste Symptome zeigen sich im 3. bis 4. Lebensmonat; unbehandelt verläuft die Erkrankung in der Regel im frühen Kindesalter letal (8; 9).
Warum HSZT?
Trotz maßgeblicher Verbesserungen in der Versorgung von Patientinnen und Patienten mit Hämoglobinopathien bleibt die allogene HSZT aktuell die einzige verfügbare kurative Therapieoption. Hämatopoetische Stammzellen (HSCs) befinden sich in den Nischen des Knochenmarks (BM) und bilden lebenslang die peripheren Blutzellen. Somit kann der Austausch durch gesunde Spenderinnen-/Spender-HSCs bei einer angeborenen hämatologischen Erkrankung wie Beta-Thalassämie und Sichelzellkrankheit zu einer Heilung führen.
Die Hauptindikation für eine HSZT bei Thalassämie-Patientinnen und -Patienten ist die Transfusionsabhängigkeit. Bei allen Kindern mit transfusionsabhängiger Thalassämie, die eine/n verfügbare/n gesunde/n HLA-identische/n verwandte/n Spenderin/Spender (in der Regel ein Geschwister) haben, sollte die HSZT so früh wie möglich angeboten werden (10). Um das Risiko von Komplikationen im Verlauf der HSZT einschätzen zu können, hat die Pesaro-Gruppe einen prognostischen Score für Patientinnen und Patienten unter 17 Jahren entwickelt und sie in 3 Risikogruppen eingeteilt, wobei die adäquate Eisenchelation, die Hepatomegalie und die portale Fibrose berücksichtigt wurden (11).
Da die klinischen Phänotypen der Sichelzellkrankheit variieren, sind die Indikationen für eine HSZT bei Patientinnen und Patienten mit Sichelzellkrankheit, im Gegensatz zu jenen mit Thalassämie, nicht universell definiert. Eine der allgemein akzeptierten Indikationen für HSZT bei Sichelzellkrankheit ist die Erkrankung des zentralen Nervensystems – verbunden mit dem Risiko wiederkehrender oder fortschreitender zerebraler Infarkte – trotz angemessener Transfusionstherapie. Andere schwere Komplikationen wie Osteonekrosen, pulmonale Hypertonie, Sichelzellnephropathie, rezidivierende venöse okklusive Krisen, akutes Thoraxsyndrom und Milzsequestrationskrise können ebenfalls als Indikationen für HSZT in Betracht gezogen werden, da sie mit einer erheblichen Morbidität und Beeinträchtigung der Lebensqualität einhergehen.
Die präventiven Strategien zusammen mit der Behandlung mit Hydroxycarbamid haben in den letzten zwei Jahrzehnten zu erheblichen Verbesserungen der Überlebenschancen von Kindern beigetragen. Dennoch ist die Mortalität bei erwachsenen Patientinnen und Patienten erheblich. Die HSZT von einem HLA-identischen Geschwisterkind ist Therapiestandard bei Patientinnen und Patienten mit Sichelzellkrankheit und mit einem ereignisfreien Überleben (EFS) nach 5 Jahren von 91,4 % und einem Gesamtüberleben (OS) nach 5 Jahren von 92,9 % vergesellschaftet. Die Erfahrungen mit HSZT von passenden Fremd- und haploidentischen Spenderinnen und Spendern bei Patientinnen und Patienten mit Sichelzellkrankheit sind demgegenüber gering (10; 12; 13).

Wann sollte bei welchen Patientinnen und Patienten eine HSZT erwogen werden?
In den letzten Jahren haben eine Reihe von Faktoren, darunter die verbesserte Vorbereitung und Prävention der Graft-versus-Host-Erkrankung (GvHD) sowie effektivere antibakterielle, antivirale und antimykotische Behandlungen, zu einer signifikanten Verbesserung der HSZT-Ergebnisse geführt, wodurch heute bei 80 bis 90 % der Patientinnen und Patienten eine Heilung der Thalassämie erreicht wird.
Die Indikation zur HSZT bei transfusionsabhängiger Thalassämie (TDT) ist immer gegeben! Die HSZT sollte Thalassämie-Patientinnen und -Patienten und ihren Eltern in einem jungen Alter angeboten werden (Vorschulalter), also bevor Komplikationen aufgrund von Eisenüberladung auftreten, insbesondere wenn ein HLA-identisches Geschwister verfügbar ist. Ein passender Fremdspender bzw. eine passende Fremdspenderin kann in Anspruch genommen werden, vorausgesetzt, dass eine hohe Kompatibilität sowohl für HLA-Klasse-I- wie auch für HLA-Klasse-II-Loci (9 oder 10 von 10) besteht. Eine HSZT von einer haploidentischen Familienspenderin/einem haploidentischen Familienspender (in der Regel einem Elternteil) kann in erfahrenen HSZT-Zentren im Rahmen gut gestalteter klinischer Studien in Betracht gezogen werden (10-13). Auch bei der Sichelzellkrankheit sollte eine HSZT durchgeführt werden, bevor die Organe durch die Grunderkrankung geschädigt werden und sich damit das Risiko von Transplantationskomplikationen und die Transplantationsmortalität erhöhen. Jedoch sind der Verlauf der Sichelzellerkrankung und das Auftreten von Komplikationen sehr variabel und meist nicht vorhersehbar. OS und EFS von Patientinnen und Patienten mit Sichelzellkrankheit sind nach HSZT von einem HLA-identischen Geschwisterkind im Kleinkindalter ausgezeichnet und verschlechtern sich mit zunehmendem Alter. Auch Komplikationen der Sichelzellkrankheit wie Organinfarkte mit nachfolgender Funktionsstörung treten mit zunehmendem Alter vermehrt auf und führen zu einer eingeschränkten Lebensqualität. Aus diesen Gründen gilt die HSZT bei Patientinnen und Patienten mit Sichelzellkrankheit bei Vorhandensein einer/m HLA-identischen Geschwisterspenderin/-spender als Therapiestandard und sollte so früh wie möglich (idealerweise im Vorschulalter) durchgeführt werden. Die Familie sollte detailliert über die Chancen und Risiken der HSZT wie auch der konventionellen Therapie aufgeklärt werden. Sollte kein HLA-identischer Geschwister als Stammzellspenderin/-spender vorhanden sein, ergeben sich die Dringlichkeit zur Durchführung einer HSZT und damit die Indikation zur Initiierung der Fremdspendersuche jeweils aus der individuellen Situation und der klinischen Symptomatik der Patientinnen und Patienten (10; 12-14).
Im Februar 2024 hat die EU-Kommission die bedingte Zulassung für Exagamglogene autotemce (Casgevy®) bei transfusionsabhängiger
Beta-Thalassämie und schwerer Sichelzellanämie ab dem Alter von 12 Jahren erteilt. Bei der Herstellung von „Exagamglogene autotemce“ wird die Genschere CRISPR/Cas9 verwendet.
Ablauf HSZT inklusive Nachsorge und Transition
Bei Patientinnen und Patienten mit Thalassämie kommen aufgrund der zahlreichen Transfusionen und des hyperplastischen Knochenmarks bevorzugt myeloablative Vorbereitungsregimes zum Einsatz. Treosulfan- und Busulfan-basierte Konditionierungen werden aktuell zumeist verwendet. Anti-Thymozytenglobulin (ATG) wird als Abstoßungs- und GVHD-Prophylaxe eingesetzt. Die Pesaro-Gruppe berichtete bei Thalassämie-Patientinnen und Patienten mit hohem Risiko (Klasse 3) über gute Ergebnisse nach intensiven Transfusionen zwischen Tag -45 und Tag -11 (bezogen auf die Stammzellinfusion an Tag 0), Gabe von Hydroxyurea (HU) und Azathioprin sowie intensiver Chelation mit Deferoxamin während dieses Zeitraums. Das Thalassämie-freie Überleben nach HSZT liegt bei 90 %. Mögliche Beeinträchtigungen der Lebensqualität nach Transplantation entstehen durch die Abstoßung des Transplantats und die Entwicklung einer GVHD. Letztere bestimmt maßgeblich die Morbidität nach einer HSZT. Die Entwicklung von gemischtem Chimärismus in der frühen Phase nach HSZT ist mit hohem Risiko einer Abstoßung des Transplantats verbunden (10-12; 15).
Bei Patientinnen und Patienten mit einer Sichelzellkrankheit werden intensitätsreduzierte Konditionierungen empfohlen, um die transplantationsbedingte Toxizität zu minimieren und langfristige Nebenwirkungen zu vermeiden, insbesondere bei Jugendlichen und Erwachsenen. Bei diesen Patientinnen und Patienten werden nicht-myeloablative, Melphalan-basierte Konditionierungsprotokolle an-
gewendet. Bei Patientinnen und Patienten unter 16 Jahren sind myeloablative Konditionierungen im Einsatz, wobei Treosulfan anstelle von Busulfan verwendet wird, um das Risiko eines Sinusoidalen Obstruktiven Syndroms (SOS)/Veno-Occlusive Disease (VOD) zu verringern (16; 17).
Die Eisenüberladung, die vor der HSZT infolge der Grunderkrankung (ineffektive Erythropoese, Transfusionen) entstanden ist, besteht nach der HSZT weiter und erhöht langfristig das Risiko einer Leberfibrose, Zirrhose, Kardiomyopathie und endokriner Komplikationen. Die Eisenbelastung kann durch Aderlässe (Phlebotomie; 6 ml/kg Körpergewicht in 2-3-wöchigen Intervallen) oder durch eine Chelattherapie verringert werden. Der Beginn der Phlebotomien ist nach dem Absetzen der Immunsuppressiva und frühestens 6 Monate nach der Transplantation vorgesehen. In Bezug auf mögliche endokrine Ausfälle, die auch nach einer erfolgreichen Transplantation auftreten, kann keine endgültige Aussage dazu getroffen werden, ob diese mit der Transplantation oder der Grunderkrankung in Zusammenhang stehen (18).
Zukunftsperspektive Gentherapie?
Aktuell werden Gentherapiestrategien entwickelt, die auf der Transduktion hämatopoetischer Stammzellen mit lentiviralen Vektoren und der nachfolgenden Transplantation der genetisch modifizierten Stammzellen basieren. Dadurch werden die Expression einer korrigierten Beta-Globin-Kette oder Reaktivierung der fötalen Globinsynthese und Reexpression des fötalen Hämoglobins (HbF) in den Erythrozyten, die sich aus den transduzierten Stammzellen ableiten, ermöglicht. Die Gentherapie ist eine kurative Perspektive gerade für die Patientinnen und Patienten mit Sichelzellkrankheit oder Beta-Thalassämie, für die kein/e geeignete/r Stammzellspender/in zur Verfügung steht. Posttransplantationskomplikationen wie die GVHD könnten vermieden werden (19).
Im Februar 2024 hat die EU-Kommission die bedingte Zulassung für Exagamglogene autotemce
(Casgevy®) bei transfusionsabhängiger Beta-Thalassämie und schwerer Sichelzellanämie ab dem Alter von 12 Jahren erteilt. Bei der Herstellung von „Exagamglogene autotemce“ wird die Genschere CRISPR/Cas9 verwendet. Zunächst werden der Patientin/dem Patienten Stammzellen entnommen, welche mittels CRISPR/Cas9 genetisch modifiziert werden. Diese Modifikation hat die Blockierung des Gens BCL11A zum Ziel, was die Expression von HbF hemmt. Im weiteren Verlauf erhält die Patientin/der Patient eine Chemotherapie, gefolgt von der Gabe der modifizierten Stammzellen. Nach erfolgreichem Engraftment der modifizierten Stammzellen wird in den sich ableitenden Erythrozyten HbF exprimiert und der Anteil der krankheitsverursachenden Globinketten vermindert.
Die bisherigen Studien zeigen vielversprechende Ergebnisse bei jedoch bislang begrenzter Zahl von Studienteilnehmerinnen und -teilnehmern und kurzem Nachbeobachtungszeitraum (20; 21).
Daneben befinden sich viral modifizierte Stammzellen sowohl für Patientinnen und Patienten mit Thalassämien (Betibeglogene autotemcel, Zenteglo) als auch für diejenigen mit SCD (Lovotibeglogene Autotemcel) in der klinischen Erprobung oder sind bereits für sehr enge Indikationen zugelassen. Analog zur allogenen SZT muss vor der Applikation dieser genetisch modifizierten, kostenintensiven Zellprodukte eine myeloablative Behandlung mit all ihren möglichen Komplikationen erfolgen.
Versorgung von Kindern und Jugendlichen mit Hämoglobinopathien in Sachsen-Anhalt
Pädiatrische Patientinnen und Patienten mit Hämoglobinopathien in Sachsen-Anhalt werden an zwei spezialisierten Standorten, dem Universitätsklinikum Magdeburg und dem Universitätsklinikum Halle (Saale), in den jeweiligen Kliniken für Pädia-trische Hämatologie und Onkologie betreut. Diese beiden Einrichtungen stellen sicher, dass eine umfassende interdisziplinäre Betreuung gewährleistet ist, die sowohl die chronische Therapie als auch die Notfallversorgung umfasst. Der multidisziplinäre Ansatz beinhaltet unter anderem die Durchführung von chronischen Transfusionsprogrammen, die Anpassung der Chelattherapie, die Behandlung von Sichelzellkrisen sowie die Therapie akuter Komplikationen und Organdysfunktionen. Zusätzlich werden die betroffenen Familien von einem psychosozialen Team eng begleitet, um die Behandlung optimal zu unterstützen.
Einmal wöchentlich wird in einem gemeinsamen Hämatopoetischen Stammzelltransplantations-Board (HSZT-Board) die Indikation zur Stammzelltransplantation diskutiert und deren Durchführung im Detail geplant. Dieser regelmäßige Dialog zwischen beiden Zentren ermöglicht darüber hinaus auch einen kontinuierlichen Austausch über etwaige Komplikationen während des Posttransplantationsverlaufes. Die Entscheidung zur HSZT wird patientenindividuell und mit äußerster Sorgfalt auf Grundlage der aktuellen klinischen Daten getroffen.
Vor einer geplanten Stammzelltransplantation sind neben einer gründlichen Organdiagnostik häufig auch vorbereitende therapeutische Maßnahmen notwendig. Diese werden in enger Abstimmung an den jeweiligen Standorten der Universitätskliniken in Halle (Saale) und Magdeburg durchgeführt. Die Stammzelltransplantation selbst findet im Transplantationsbereich des Universitätsklinikums Halle (Saale) in Zusammenarbeit mit der Universitätsklinik und Poliklinik für Innere Medizin IV (Hämatologie, Onkologie und Stammzelltransplantation) des Universitätsklinikums Halle (Saale) statt. Die Nachsorge nach der Transplantation wird heimatnah in Magdeburg oder Halle (Saale) fortgesetzt, so dass die Patientinnen und Patienten auch während der Posttransplantationsphase eine optimale Versorgung erhalten. Durch die enge Kooperation zwischen den Universitätskliniken Magdeburg und Halle (Saale) wird patientenindividuell die bestmögliche Behandlung der betroffenen Patientinnen und Patienten und ihrer Familien gewährleistet.
Die neuen gentherapeutischen Verfahren stehen derzeit in Sachsen-Anhalt noch nicht zur Verfügung, der Einsatz dieser neuen Verfahren wird geplant.
Literaturverzeichnis
- Kattamis A, Kwiatkowski JL, Aydinok Y Thalassaemia. Lancet (2022); 399 2310-2324. doi:10.1016/s0140-6736(22)00536-0
- Kohne E. (2011). Hemoglobinopathies: clinical manifestations, diagnosis, and treatment. Deutsches Arzteblatt international, 108(31-32), 532–540.
- Forni, G. L., Gianesin, B., Musallam, K. M., Longo, F., Rosso, R., Lisi, R., Gamberini, M. R., Pinto, V. M., Graziadei, G., Vitucci, A., Bonetti, F., Musto, P., Piga, A., Cappellini, M. D., Borgna-Pignatti, C., & Webthal® project (2023). Overall and complication-free survival in a large cohort of patients with β-thalassemia major followed over 50 years. American Journal of Hematology, 98(3), 381–387.
- Modell, B., Khan, M., & Darlison, M. (2000). Survival in beta-thalassaemia major in the UK: data from the UK Thalassaemia Register. Lancet (London, England), 355(9220), 2051–2052.
- Gemeinsamer Bundesausschuss (2021). Abschlussbericht. Kinder-Richtlinie: Screening auf Sichelzellkrankheit bei Neugeborenen. Verfügbar unter: https://www.g-ba.de/beschluesse/4560/ Veröffentlicht am 29.03.2021. Zugriff am 03.11.2024
- Kato, G. J., Piel, F. B., Reid, C. D., Gaston, M. H., Ohene-Frempong, K., Krishnamurti, L., Smith, W. R., Panepinto, J. A., Weatherall, D. J., Costa, F. F., & Vichinsky, E. P. (2018). Sickle cell disease. Nature Reviews. Disease primers, 4, 18010.
- Gesellschaft für Pädiatrische Onkologie und Hämatologie. AWMF-S2k-Leitlinie 025/016 „Sichelzellkrankheit“. 2. Auflage vom 2. Juli 2020. Verfügbar unter: https://www.awmf.org/leitlinien/detail/ll/025-016.html. Zugriff am 03.11.2024
- Rees, D. C., Williams, T. N., & Gladwin, M. T. (2010). Sickle-cell disease. Lancet (London, England), 376(9757), 2018–2031. https://doi.org/10.1016/S0140-6736(10)61029-X
- Brandow, A. M., & Liem, R. I. (2022). Advances in the diagnosis and treatment of sickle cell disease. Journal of hematology & oncology, 15(1), 20.
- Yesilipek, M. A. (2020). Hematopoietic Stem Cell Transplantation in Patients with Hemoglobinopathies. Hemoglobin, 44(6), 377–384. https://doi.org/10.1080/03630269.2020.1832516
- Sodani, P., Gaziev, D., Polchi, P., Erer, B., Giardini, C., Angelucci, E., Baronciani, D., Andreani, M., Manna, M., Nesci, S., Lucarelli, B., Clift, R. A., & Lucarelli, G. (2004). New approach for bone marrow transplantation in patients with class 3 thalassemia aged younger than 17 years. Blood, 104(4), 1201–1203. https://doi.org/10.1182/blood-2003-08-2800
- Lucarelli, G., Isgrò, A., Sodani, P., & Gaziev, J. (2012). Hematopoietic stem cell transplantation in thalassemia and sickle cell anemia. Cold Spring Harbor Perspectives in Medicine, 2(5), a011825. https://doi.org/10.1101/cshperspect.a011825
- Angelucci, E., Matthes-Martin, S., Baronciani, D., Bernaudin, F., Bonanomi, S., Cappellini, M. D., Dalle, J. H., Di Bartolomeo, P., de Heredia, C. D., Dickerhoff, R., Giardini, C., Gluckman, E., Hussein, A. A., Kamani, N., Minkov, M., Locatelli, F., Rocha, V., Sedlacek, P., Smiers, F., Thuret, I., … EBMT Inborn Error and EBMT Paediatric Working Parties (2014). Hematopoietic stem cell transplantation in thalassemia major and sickle cell disease: indications and management recommendations from an international expert panel. Haematologica, 99(5), 811–820. https://doi.org/10.3324/haematol.2013.099747
- Jang, T., Mo, G., Stewart, C., Khoury, L., Ferguson, N., Egini, O., Muthu, J., Dutta, D., Salifu, M., & Lim, S. H. (2021). Hematopoietic Stem Cell Transplant for Sickle Cell Disease: PATIENT SELEction and Timing Based on Sickle Cell-Related Multiple Chronic Conditions. Cell transplantation, 30, 9636897211046559. https://doi.org/10.1177/09636897211046559
- Huang, K., Zhou, D. H., Li, Y., Xu, H. G., Que, L. P., Chen, C., Xue, H. M., Guo, H. X., Weng, W. J., Huang, S. L., & Fang, J. P. (2018). Modified conditioning regimen improves outcomes of unrelated donor peripheral blood stem cell transplantation for β-thalassaemia major patients. Pediatric Blood & Cancer, 65(7), e27026. https://doi.org/10.1002/pbc.27026
- Kanter, J., Liem, R. I., Bernaudin, F., Bolaños-Meade, J., Fitzhugh, C. D., Hankins, J. S., Murad, M. H., Panepinto, J. A., Rondelli, D., Shenoy, S., Wagner, J., Walters, M. C., Woolford, T., Meerpohl, J. J., & Tisdale, J. (2021). American Society of Hematology 2021 guidelines for sickle cell disease: stem cell transplantation. Blood Advances, 5(18), 3668–3689. https://doi.org/10.1182/bloodadvances.2021004394C
- Strocchio, L., Zecca, M., Comoli, P., Mina, T., Giorgiani, G., Giraldi, E., Vinti, L., Merli, P., Regazzi, M., & Locatelli, F. (2015). Treosulfan-based conditioning regimen for allogeneic haematopoietic stem cell transplantation in children with sickle cell disease. British Journal of Haematology, 169(5), 726–736. https://doi.org/10.1111/bjh.13352
- Aboobacker, F. N., Dixit, G., Lakshmi, K. M., Korula, A., Abraham, A., George, B., Mathews, V., & Srivastava, A. (2021). Outcome of iron reduction therapy in ex-thalassemics. PloS One, 16(1), e0238793. https://doi.org/10.1371/journal.pone.0238793
- Locatelli, F., Cavazzana, M., Frangoul, H., Fuente, J., Algeri, M., & Meisel, R. (2024). Autologous gene therapy for hemoglobinopathies: From bench to patient's bedside. Molecular therapy : the journal of the American Society of Gene Therapy, 32(5), 1202–1218. https://doi.org/10.1016/j.ymthe.2024.03.005
- Frangoul, H., Locatelli, F., Sharma, A., Bhatia, M., Mapara, M., Molinari, L., Wall, D., Liem, R. I., Telfer, P., Shah, A. J., Cavazzana, M., Corbacioglu, S., Rondelli, D., Meisel, R., Dedeken, L., Lobitz, S., de Montalembert, M., Steinberg, M. H., Walters, M. C., Eckrich, M. J., … CLIMB SCD-121 Study Group (2024). Exagamglogene Autotemcel for Severe Sickle Cell Disease. The New England Journal of Medicine, 390(18), 1649–1662. https://doi.org/10.1056/NEJMoa2309676
- Locatelli, F., Lang, P., Wall, D., Meisel, R., Corbacioglu, S., Li, A. M., de la Fuente, J., Shah, A. J., Carpenter, B., Kwiatkowski, J. L., Mapara, M., Liem, R. I., Cappellini, M. D., Algeri, M., Kattamis, A., Sheth, S., Grupp, S., Handgretinger, R., Kohli, P., Shi, D., … CLIMB THAL-111 Study Group (2024). Exagamglogene Autotemcel for Transfusion-Dependent β-Thalassemia. The New England Journal of Medicine, 390(18), 1663–1676. https://doi.org/10.1056/NEJMoa2309673
Korrespondierender Autor:
Kinan Kafa
E-Mail:
Universitätsklinikum Halle (Saale)
Universitätsklinik und Poliklinik für Pädiatrie I
Ernst-Grube-Straße 40
06120 Halle (Saale)
Weitere Artikel
Weiterlesen … Fachbeitrag 06/2025 - Kurative Behandlung von Hämoglobinopathien in Sachsen-Anhalt
- Aufrufe: 2219